

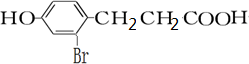 .
.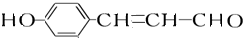 +2[Ag(NH3)2]OH$\stackrel{△}{→}$
+2[Ag(NH3)2]OH$\stackrel{△}{→}$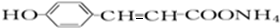 +2Ag↓+3NH3+H2O,反應類型為氧化反應.
+2Ag↓+3NH3+H2O,反應類型為氧化反應.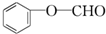 ,
, .
. +2nH2O.
+2nH2O. 分析 A能發生顯色反應說明A中含有酚羥基,A能和銀氨溶液反應說明含有醛基;A發生銀鏡反應生成C、C酸化生成D、D發生加成反應生成E,A中含有醛基和酚羥基,則A中至少含有2個O原子,則從A到E碳原子個數不變、O原子個數增多1個、H原子個數增多2個,則A的分子式為C9H8O2,A的不飽和度=$\frac{9×2+2-8}{2}$=6,苯環的不飽和度為4、醛基的不飽和度為1,則A中還含有一個碳碳雙鍵;
A和2mol氫氣發生加成反應生成B,B中不含甲基,則A的結構簡式為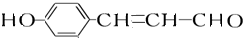 ,B結構簡式為
,B結構簡式為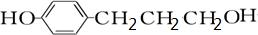 ,A中醛基被氧化生成羧酸銨,C結構簡式為
,A中醛基被氧化生成羧酸銨,C結構簡式為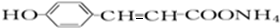 ,C酸化得到D,D結構簡式為
,C酸化得到D,D結構簡式為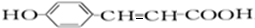 ,D和1mol氫氣發生加成反應生成E,E結構簡式為
,D和1mol氫氣發生加成反應生成E,E結構簡式為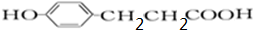 ,E和溴發生取代反應生成F,F僅有一種結構,結合F分子式知F結構簡式為
,E和溴發生取代反應生成F,F僅有一種結構,結合F分子式知F結構簡式為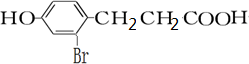 ,據此分析解答.
,據此分析解答.
解答 解:A能發生顯色反應說明A中含有酚羥基,A能和銀氨溶液反應說明含有醛基;A發生銀鏡反應生成C、C酸化生成D、D發生加成反應生成E,A中含有醛基和酚羥基,則A中至少含有2個O原子,則從A到E碳原子個數不變、O原子個數增多1個、H原子個數增多2個,則A的分子式為C9H8O2,A的不飽和度=$\frac{9×2+2-8}{2}$=6,苯環的不飽和度為4、醛基的不飽和度為1,則A中還含有一個碳碳雙鍵;
A和2mol氫氣發生加成反應生成B,B中不含甲基,則A的結構簡式為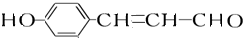 ,B結構簡式為
,B結構簡式為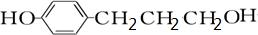 ,A中醛基被氧化生成羧酸銨,C結構簡式為
,A中醛基被氧化生成羧酸銨,C結構簡式為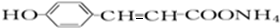 ,C酸化得到D,D結構簡式為
,C酸化得到D,D結構簡式為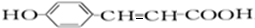 ,D和1mol氫氣發生加成反應生成E,E結構簡式為
,D和1mol氫氣發生加成反應生成E,E結構簡式為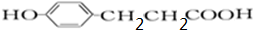 ,E和溴發生取代反應生成F,F僅有一種結構,結合F分子式知F結構簡式為
,E和溴發生取代反應生成F,F僅有一種結構,結合F分子式知F結構簡式為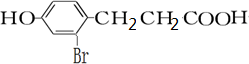 ,
,
(1)通過以上分析知,A的分子式為C9H8O2,F結構簡式為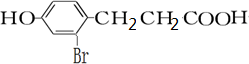 ,
,
故答案為:C9H8O2;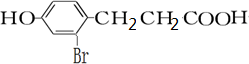 ;
;
(2)A的結構簡式為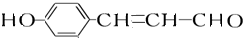 、C結構簡式為
、C結構簡式為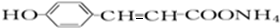 ,A發生銀鏡反應生成C,反應方程式為
,A發生銀鏡反應生成C,反應方程式為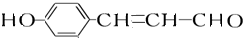 +2[Ag(NH3)2]OH$\stackrel{△}{→}$
+2[Ag(NH3)2]OH$\stackrel{△}{→}$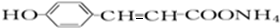 +2Ag↓+3NH3+H2O,該反應為氧化反應,
+2Ag↓+3NH3+H2O,該反應為氧化反應,
故答案為: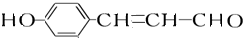 +2[Ag(NH3)2]OH$\stackrel{△}{→}$
+2[Ag(NH3)2]OH$\stackrel{△}{→}$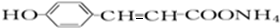 +2Ag↓+3NH3+H2O;氧化反應;
+2Ag↓+3NH3+H2O;氧化反應;
(3)B為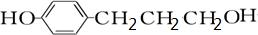 ,B的同分異構體符合下列條件:①1mol物質最多能消耗3molBr2②苯環上只有兩個取代基③分子中只出現一個-CH3的結構,
,B的同分異構體符合下列條件:①1mol物質最多能消耗3molBr2②苯環上只有兩個取代基③分子中只出現一個-CH3的結構,
如果取代基為-OH、-CH2CH(OH)CH3且二者處于間位時符合條件,有一種結構,;
如果取代基為-OH、-CH(OH)CH2 CH3且二者處于間位時符合條件,有一種結構;
如果取代基為-OH、-CH(CH3)CH2OH且二者處于間位時符合條件,有一種結構;
所以符合條件的有三種同分異構體,
故答案為:3;
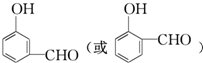
(4)一定條件下R1CH═CHR2→R1CHO+R2CHO,A在一定條件下氧化生成X、Y(A中酚羥基已被保護),X的分子式為C7H6O2,它是芳香族化合物,X為 ,Y可進一步氧化得到一種還原性的二元羧酸,Y為OHCCHO,
,Y可進一步氧化得到一種還原性的二元羧酸,Y為OHCCHO,
①X為 ,X的同分異構體中含有醛基,其同分異構體中可能存在-CHO、-OH且二者位于鄰位或間位,可能存在-O-CHO,符合條件的結構簡式有
,X的同分異構體中含有醛基,其同分異構體中可能存在-CHO、-OH且二者位于鄰位或間位,可能存在-O-CHO,符合條件的結構簡式有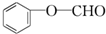 、
、 ,
,
故答案為: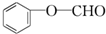 ;
; ;
;
②Y被氧化得到的乙二酸與乙二醇發生酯化反應形成高分子化合物的化學方程式為
nHOCH2CH2OH+nHOOC-COOH$?_{△}^{濃硫酸}$ +2nH2O,
+2nH2O,
故答案為:nHOCH2CH2OH+nHOOC-COOH$?_{△}^{濃硫酸}$ +2nH2O.
+2nH2O.
點評 本題考查有機物推斷,側重考查學生分析推斷能力,為高考高頻點,正確推斷A的結構簡式是解本題關鍵,再結合反應物的量、反應條件、某些物質的分子式進行推斷,難點是同分異構體種類的判斷,注意乙二酸和乙二醇發生縮聚反應中水的計量數,為易錯點.


 全能測控一本好卷系列答案
全能測控一本好卷系列答案科目:高中化學 來源: 題型:選擇題
| A. | 0.06mol•L-1•min-1 | B. | 0.001mol•L-1•s-1 | ||
| C. | 0.04mol•L-1•min-1 | D. | 0.0005mol•L-1•s-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
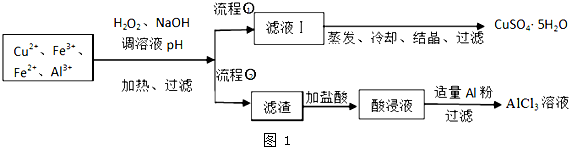
| 離子 | Fe3+ | Fe2+ | Al3+ | Cu2+ |
| pH范圍 | 2.2~3.2 | 5.5~9.0 | 4.1~5.0 | 5.3~6.6 |
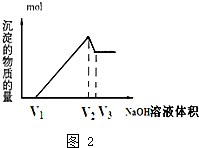
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 成份 | 濃度/(mol•L-1) | 質量分數 |
| HCl FeCl2 FeCl3 | -- 1.920 0.071 | 5.00% 8.94% 0.33% |
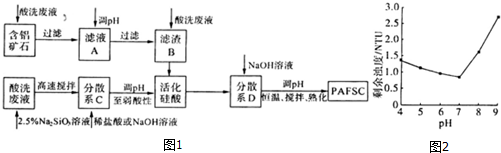
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 5.0 m o l/L | B. | 4.0 m o l/L | C. | 4.5 m o l/L | D. | 3.0 m o l/L |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①④⑤ | B. | ②③④⑤⑥ | C. | ④⑤⑥⑦ | D. | 全部 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 對于元素周期表和元素周期律的發現有突出貢獻的科學家是阿伏加德羅 | |
| B. | 元素周期表根據相對原子質量從小到大的順序排列 | |
| C. | 現常見的元素周期表有七個橫行,分為七個周期,有18個縱行,分為16個族 | |
| D. | 每一周期都是從金屬元素開始,非金屬元素結束 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 核外電子是分層運動的,像衛星一樣有確定的軌道 | |
| B. | 所有電子在同一區域里運動 | |
| C. | 能量高的電子在離核近的區域運動 | |
| D. | 能量低的電子在離核近的區域運動 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com