人們經常用電化學的基本理論和測定方法求算一些熱力學函數變化值,或用已知的熱力學函數值來求得電化學反應的物理量,這些理論和方法的應用給解決實際問題帶來極大方便.
現設計以下電池(298K,p
Θ)
(-)(Pt)Cl
2(g,p
Θ)|HCl(1mol/dm
3)|AgCl(s)-Ag(s)(+)
其中Cl
-1|AgCl(s)-Ag(s)電極稱為銀-氯化銀電極,是微溶鹽電極,其電極反應為:AgCl(s)+e
-→Ag(s)+Cl
-(1mol/dm
3),是對Cl
-的可逆電極.
已知有關物質的熱力學數據如下:
| 物質 | △fHΘm/kJ?mol-1 | SΘm/J?mol-1?K-1 |
| AgCl (s) | -127.0 | 96.11 |
| Ag (s) | 0 | 42.70 |
| Cl2 (g) | 0 | 223.0 |
法拉第常數 F=9.65×10
4 C?molˉ
1,理想氣體常數R=8.314J?molˉ
1?Kˉ
1(1)根據該電池正、負極的電極反應,寫出該電池的電池反應式
(2)求該反應的△
rH
Θm和△
rS
Θm和△
rG
Θm,(298K,p
Θ)
(3)求該電池反應的電動勢E及標準電池電動勢E
Θ.已知△
rG
Θm=-nFE
Θ;
△
rG=-nFE,其中n為電極反應得失電子的物質的量.
(4)求該電池在可逆放電時的熱效應Q
R.Q
R等于該反應的△
rΗ
Θm嗎?為什么?
(5)已知恒壓下△
rS
Θm=nF(△E/△T),(△E/△T)為電池電動勢的溫度系數,試求之?
(6)求該電池反應的平衡常數K
Θ.
(7)根據題(3)中求得的E
Θ和E的數值,能否判斷所設計的電池是自發電池還是非自發電池?若想改變方向,如何進行操作?

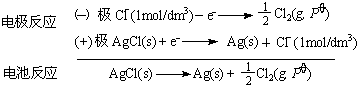 ,
,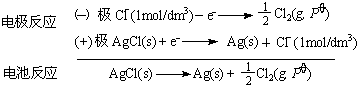 ;
;

 陽光課堂同步練習系列答案
陽光課堂同步練習系列答案 按要求回答下列問題.
按要求回答下列問題.