
分析 (1)依據蓋斯定律計算反應熱,寫出反應的熱化學方程式;
(2)令CO的濃度變化為c,用三段式表示出各物質變化的濃度、平衡時的濃度,再根據平衡常數計算;
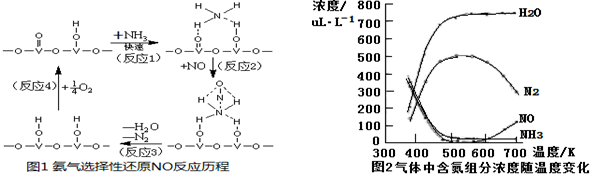
(3)①用V2O5作催化劑,NH3可將NO還原成N2,結合反應歷程圖可知反應物還有氧氣,生成物為N2和H2O,配平即得反應方程式;
②由該反應的平衡常數與溫度的關系lg Kp=5.08+217.5/T,平衡常數是溫度的減函數,即升高溫度,化學反應逆向移動,所以該反應是放熱反應;
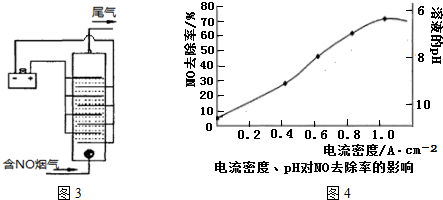
③由圖2分析,當溫度達到700K時,與500K-600K比較,相同氨氣形成相同水的時,生成的N2在減少,NO在增加,說明氨催化氧化生成了NO,故此時的副反應產物是NO.
(4)①食鹽水做電解液電解煙氣(Cl2)脫氮,根據氧化還原反應的規律可得反應;
②次氯酸鈉在酸性條件下氧化性增強,故溶液的pH對NO去除率會有影響;
③根據電荷量(Q)=電流密度×極板面積×時間=n(e-)?F,可知NO除去率.
解答 解:(1)依據蓋斯定律將CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ•mol-1與CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H2=-1160kJ•mol-1兩方程式相加后再除以2,得2NO2(g)+CH4(g)=N2(g)+CO2(g)+2H2O(g)△H=-867kJ•mol-1,故答案為:2NO2(g)+CH4(g)=N2(g)+CO2(g)+2H2O(g)△H=-867 kJ•mol-1;
(2)對于反應 CO(g)+H2O(g)  H2(g)+CO2(g),
H2(g)+CO2(g),
開始(mol/L):0.02 0.02 0 0
變化(mol/L):c c c c
平衡(mol/L):0.02-c 0.02-c c c
所以$\frac{c×c}{(0.02-c)×(0.02-c)}$=9,解得c=0.015
所以CO的轉化率為$\frac{0.015mol/L}{0.02mol/L}$×100%=75%.
故答案為:75%.
(3)①用V2O5作催化劑,NH3可將NO還原成N2,結合反應歷程圖可知反應物還有氧氣,生成物為N2和H2O,配平即得反應方程式為4NH3+4NO+O2$\frac{\underline{\;V_{2}O_{5}\;}}{\;}$4N2+6H2O,故答案為:4NH3+4NO+O2$\frac{\underline{\;V_{2}O_{5}\;}}{\;}$4N2+6H2O;
②平衡常數是溫度的減函數,則該反應是為放熱反應,故答案為:放熱;
③由圖2分析,當溫度達到700K時,生成的N2在減少,NO在增加,說明氨催化氧化生成了NO,故此時的副反應是:4NH3+5O2 4$\frac{\underline{催化劑}}{△}$NO+6H2O,故答案為:4NH3+5O2 $\frac{\underline{催化劑}}{△}$4NO+6H2O;
(4)①氯氣作氧化劑,NO為還原劑,在堿性條件下的反應為:3Cl2+8OH-+2NO=2NO3-+6Cl-+4H2O,故答案為:3Cl2+8OH-+2NO=2NO3-+6Cl-+4H2O;
②次氯酸鈉在酸性條件下氧化性增強,故溶液的pH對NO去除率會有影響,故答案為:次氯酸鈉在酸性條件下氧化性增強;
③根據電荷量(Q)=電流密度×極板面積×時間=n(e-)?F,NO除去率:$\frac{\frac{1.0A.c{m}^{-2}×1s×10c{m}^{2}}{96500c.mo{l}^{-1}×3}}{\frac{0.070L.{s}^{-1}×15%}{22.4L.mo{l}^{-1}}}$×100%=73.7%,故答案為:$\frac{\frac{1.0A.c{m}^{-2}×1s×10c{m}^{2}}{96500c.mo{l}^{-1}×3}}{\frac{0.070L.{s}^{-1}×15%}{22.4L.mo{l}^{-1}}}$×100%=73.7%.
點評 本題考查了蓋斯定律求反應熱、化學平衡常數及化學平衡移動的影響因素、氧化還原反應等,題目難度中等.


 寒假學與練系列答案
寒假學與練系列答案科目:高中化學 來源: 題型:選擇題
| A. | 該反應條件下,初始時向容器中充入2molSO2和1molO2,反應平衡時,可以釋放198.0 kJ的熱量 | |
| B. | 達到平衡時,SO2和SO3的濃度一定相等 | |
| C. | 反應體系中,當混合物的密度保持不變,反應達到平衡 | |
| D. | 增大壓強和升高溫度有利于加快反應速率,但升高溫度對平衡轉化率不利 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 沸點(℃) | 密度(g•cm-3) | |
| 苯甲酸 | 249 | 1.2659 |
| 苯甲酸乙酯 | 212.6 | 1.05 |
| 乙醇 | 78.5 | 0.7893 |
| 環己烷 | 80.8 | 0.7785 |
| 乙醚 | 34.51 | 0.7318 |
| 環己烷、乙醇和水共沸物 | 62.1 |

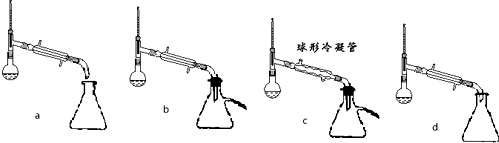
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在一定條件下,使用催化劑能加快反應速率并提高反應物的平衡轉化率 | |
| B. | 當反應達平衡時,恒溫恒壓條件下通入Ar,能提高COCl2的轉化率 | |
| C. | 單位時間內生成CO和Cl2的物質的量比為1:1時,反應達到平衡狀態 | |
| D. | 平衡時,其他條件不變,升高溫度可使該反應的平衡常數增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 保持體積不變加入H2 | B. | 壓縮體積至原來的一半 | ||
| C. | 降低溫度 | D. | 加入催化劑 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
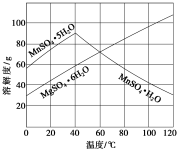 軟錳礦(主要成分MnO2,雜質金屬元素Fe、Al、Mg等)的水懸濁液與煙氣中SO2反應可制備MnSO4•H2O,反應的化學方程式為:MnO2+SO2═MnSO4.
軟錳礦(主要成分MnO2,雜質金屬元素Fe、Al、Mg等)的水懸濁液與煙氣中SO2反應可制備MnSO4•H2O,反應的化學方程式為:MnO2+SO2═MnSO4.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com