
分析 (1)根據物質的量之比等于熱量比計算出1molN2H4完全放出的熱量,依據熱化學方程式書寫方法寫出,標注物質聚集狀態和反應焓變;
(2)反應H2O2中O元素的化合價從-1價降低到-2價;
(3)根據熱化學方程式計算出放出256.65kJ熱量時,反應的雙氧水的物質的量,結合化合價的變化計算轉移電子數;
(4)根據產物的性質分析.
解答 解:(1)0.4mol液態肼與足量過氧化氫反應,生成氮氣和水蒸氣,放出256.65kJ的熱量,32g肼燃燒放熱641.625kJ;肼燃燒的熱化學方程式為:N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=-641.625kJ/mol;
故答案為:N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=-641.625kJ/mol;
(2)反應H2O2中O元素的化合價從-1價降低到-2價,H2O2得電子,作氧化劑;
故答案為:H2O2;
(3)放出256.65kJ熱量時,反應的雙氧水的物質的量為$\frac{256.65kJ}{641.625kJ/mol}$×2=0.8mol,則轉移電子的物質的量為1.6mol,轉移電子數1.6NA;
故答案為:1.6NA;
(4)肼(N2H4)和液態過氧化氫反應產生大量N2和H2O(g),并放出大量的熱量,反應產物無污染,故答案為:污染小,產生的熱量多.
點評 本題考查了反應熱的計算、熱化學方程式的書寫、氧化還原反應,題目難度不大,注意把握熱化學方程式書寫方法和氧化還原反應的原理.


科目:高中化學 來源: 題型:選擇題
| A. | Fe分別與氯氣和稀鹽酸反應所得氯化物相同 | |
| B. | 常溫下干燥的Cl2能用鋼瓶貯運,所以Cl2不與鐵反應 | |
| C. | 氯氣具有漂白性 | |
| D. | 根據較強酸可以制取較弱酸的規律,推出CO2通入NaClO溶液中能生成HClO |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向100mL0.1mol•L-1的Na2CO3溶液中滴加含0.01molCH3COOH的醋酸溶液CO32-+CH3COOH═HCO3-+CH3COO- | |
| B. | 4mol•L-1的NaAlO2溶液和7mol•L-1的鹽酸等體積均勻混合4AlO2-+7H++H2O═3Al(OH)3↓+Al3+ | |
| C. | 等物質的量的FeBr2與Cl2反應(已知:Br2+2Fe2+═2Fe3++2 Br-,Cl2+2Br-═Br2+2Cl-):2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- | |
| D. | 向NaAlO2溶液中通入過量CO2的反應:2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 二氧化碳的分子式: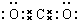 | |
| B. | Cl-的結構示意圖: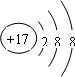 | |
| C. | 乙烯的結構簡式:CH2CH2 | |
| D. | 質子數為53、中子數為78 的碘原子:${\;}_{53}^{131}$I |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
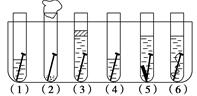 取6根鐵釘、6支潔凈試管及其他材料,按圖所示準備.
取6根鐵釘、6支潔凈試管及其他材料,按圖所示準備.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | C2H6 | B. | C2H6O | C. | C2H6O2 | D. | C3H6O3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 醫用酒精的濃度通常為75% | |
| B. | 用灼燒并聞氣味的方法區別純棉織物和純毛織物 | |
| C. | 采集某雨水樣品,放置一段時間,pH由4.8變為4.2,是因為水中溶解了較多的CO2 | |
| D. | 氫氧化鋁和碳酸氫鈉都可以作為治療胃酸過多的藥劑 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com