
分析 (1)根據2MnO4-+5H2O2+6H+═2Mn2++8H2O+5O2↑,計算每一份中H2O2的物質的量,進而計算m1 g樣品中H原子的物質的量;
(2)根據Na2CO3+BaCl2═BaCO3↓+2NaCl計算每一份中Na2CO3的物質的量,結合(1)中計算確定Na2CO3、H2O2的物質的量之比,進而確定過碳酸鈉的化學式.
解答 解:(1)由2MnO4-+5H2O2+6H+═2Mn2++8H2O+5O2↑,可知每一份中H2O2的物質的量為$\frac{5}{2}$×0.03L×0.2mol/L=0.015mol,故m1 g樣品中H原子的物質的量為0.015mol×2×2=0.06mol,
故答案為:0.06mol;
(2)由Na2CO3+BaCl2═BaCO3↓+2NaCl,可知每一份中n(Na2CO3)=n(BaCl2)=0.05L×0.2mol/L=0.01mol,Na2CO3、H2O2的物質的量之比為0.01mol:0.015mol=2:3,故過碳酸鈉的化學式為2Na2CO3•3H2O2,
故答案為:2Na2CO3•3H2O2.
點評 本題考查化學方程式有關計算,比較基礎,明確各個物理量之間的關系是解本題關鍵,側重考查分析計算能力.


 文敬圖書課時先鋒系列答案
文敬圖書課時先鋒系列答案科目:高中化學 來源: 題型:選擇題
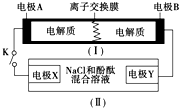 下圖為一種可充電電池的示意圖,其中的離子交換膜只允許K+通過,該電池放電、充電的化學反應方程式為:2K2S2+KI3 $?_{充電}^{放電}$K2S4+3KI.裝置(Ⅱ)為電解池的示意圖.當閉合開關K時,電極X附近溶液先變紅.則閉合K時,下列說法正確的是( )
下圖為一種可充電電池的示意圖,其中的離子交換膜只允許K+通過,該電池放電、充電的化學反應方程式為:2K2S2+KI3 $?_{充電}^{放電}$K2S4+3KI.裝置(Ⅱ)為電解池的示意圖.當閉合開關K時,電極X附近溶液先變紅.則閉合K時,下列說法正確的是( )| A. | K+從左到右通過離子交換膜 | |
| B. | 電極A上發生的反應為:3I--2e-═I3- | |
| C. | 電極X上發生的反應為:2Cl--2e-═Cl2↑ | |
| D. | 當有0.1 mol K+通過離子交換膜,X電極上產生1.12 L氣體 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氫氧化鈉溶液用帶玻璃塞的玻璃瓶存放 | |
| B. | 金屬鈉保存在水中 | |
| C. | 濃硝酸存放于無色細口瓶中 | |
| D. | 濃硫酸貯存在鋁制容器中 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向水中投入一小塊金屬鈉 | B. | 將水加熱煮沸 | ||
| C. | 向水中加入CH3COONa晶體 | D. | 向水中加入NH4Cl溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 離子半徑大小:F->Na+>Mg2+ | B. | 金屬性強弱:K>Mg>Ca | ||
| C. | 酸性強弱:HIO4>HBrO4>HClO4 | D. | 堿性強弱:LiOH>NaOH>KOH? |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 達平衡時同一物質的V(正)=V(逆) | B. | 是動態平衡 | ||
| C. | 各組分的含量不隨時間而變化 | D. | 外界條件不能改變平衡 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1 mol H2SO4與1 molBa(OH)2反應生成H2O時放出的熱叫做中和熱 | |
| B. | △H>0 kJ•mol-1表示放熱反應,△H<0 kJ•mol-1表示吸熱反應 | |
| C. | 熱化學方程式中的化學計量數表示物質的量,可以是分數 | |
| D. | 1 mol H2與0.5 mol O2反應放出的熱就是H2的燃燒熱 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 通入澄清石灰水 | |
| B. | 先通入酸性KMnO4溶液,再通入石灰水 | |
| C. | 通入品紅溶液 | |
| D. | 先通入飽和NaHCO3溶液,在通入石灰水 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com