
| A. | 負極反應式:CH3OH-8e-+8OH-=CO2+6H2O | |
| B. | 電池工作時,CH3OH發(fā)生還原反應,被氧化 | |
| C. | 電池工作時,溶液中的陰離子向負極移動 | |
| D. | 電池工作一段時間后,溶液的pH增大 |
科目:高中化學 來源: 題型:選擇題
| A. | 濃氨水、濃硝酸應保存在棕色試劑瓶中,并置于陰涼處 | |
| B. | 液溴易揮發(fā),應保存在棕色試劑瓶中,并加水封 | |
| C. | 在儲存銨態(tài)化肥時,應密封包裝并放在陰涼通風處 | |
| D. | 碘易升華,應保存在棕色細口瓶中,并置于陰涼處 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
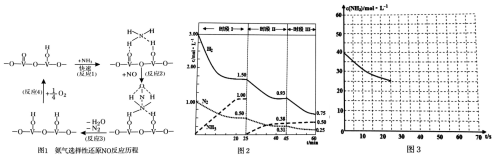
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 等于1:2 | B. | 小于1:2 | C. | 等于2:1 | D. | 大于2:1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 190 | B. | 218 | C. | 436 | D. | 463 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 無色溶液中:Na+、Cu2+、NO3-、Cl- | |
| B. | 在pH=4的溶液中:Na+、K+、OH-、Cl- | |
| C. | 在含Ba2+的溶液中:H+、Na+、Cl-、SO42- | |
| D. | 與Fe反應產生氣體的溶液:Na+、K+、Cl-、SO42- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
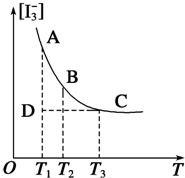 實驗室中配制碘水,往往是將I2溶于KI溶液中,這樣就可以得到濃度較大的碘水,主要是因為發(fā)生了反應:I2(aq)+I-(aq)?I3-(aq).上述平衡體系中,I3-的物質的量濃度[I3-]與溫度T的關系如圖所示(曲線上的任何一點都表示平衡狀態(tài)).
實驗室中配制碘水,往往是將I2溶于KI溶液中,這樣就可以得到濃度較大的碘水,主要是因為發(fā)生了反應:I2(aq)+I-(aq)?I3-(aq).上述平衡體系中,I3-的物質的量濃度[I3-]與溫度T的關系如圖所示(曲線上的任何一點都表示平衡狀態(tài)).查看答案和解析>>
湖北省互聯(lián)網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com