
分析 (1)依據熱化學方程式和蓋斯定律計算所需化學方程式;
(2)歧化反應磷元素升高為次磷酸鹽,磷元素化合價為+1價,降低的只能為負價,則為氫化物;
(3)H3PO4?H++H2PO4-K1=7.1×10-3;H2PO4-?H++HPO42-K2=6.3×10-8;HPO42-?H++HPO43-K3=4.2×10-13;上一級電離產生的H+對下一級電離有抑制作用;為獲得盡可能純的NaH2PO4,需H2PO4-濃度最大,根據K1、K2、以及pH=-lgc(H+)計算;
若向Na2HPO4溶液中加入足量的CaCl2溶液,HPO42-離子和Ca2+離子反應生成沉淀,促進HPO42-的電離,溶液顯示酸性;
(4)Cu元素的化合價由+2價降低到+1價,CuSO4是氧化劑,P4部分磷元素由0價降低到-3價,部分磷元素由0價升高到+5價,磷元素的化合價既升高又降低,所以P4既是氧化劑又是還原劑,若有11molP4參加反應,其中5mol的P4做氧化劑,60mol硫酸銅做氧化劑,只有6mol的P4做還原劑,結合電子守恒來解答.
解答 解:(1)①4Ca3(PO4)2(s)+10C(s)=12CaO(s)+2P4(s)+10CO2(g)△H1=+Q1kJ•mol-1
②CaO(s)+SiO2(s)=CaSiO3(s)△H2=-Q2 kJ•mol-1
③CO2(g)+C(s)=2CO(g)△H3=+Q3kJ•mol-1
依據熱化學方程式和蓋斯定律計算得到①×$\frac{1}{2}$+③+②×6得到化學方程式為:2Ca3(PO4)2+6SiO2+10C$\frac{\underline{\;高溫\;}}{\;}$6CaSiO3+P4+10CO;
故答案為:2Ca3(PO4)2+6SiO2+10C$\frac{\underline{\;高溫\;}}{\;}$6CaSiO3+P4+10CO;
(2)白磷在熱的濃氫氧化鉀溶液中岐化得到一種次磷酸鹽(KH2PO2)和一種氣體,歧化反應磷元素升高為次磷酸鹽,磷元素化合價為+1價,降低的只能為負價,則為氫化物PH3;
故答案為:PH3;
(3)為獲得盡可能純的NaH2PO4,需配制磷酸、磷酸二氫鈉的緩沖溶液,當溶液全部為磷酸溶液時,磷酸以第一步電離為主,所以H3PO4?H++H2PO4-K1=7.1×10-3;PH=-lgc(H+)=3-lg7.1≈2.1,
當溶液全部為NaH2PO4溶液時,H2PO4-?H++HPO42-K2=6.3×10-8,所以pH=-lgc(H+)=8-lg6.3≈7.2,
所以pH應控制介于2.1~7.2之間;HPO42-離子既能發生電離又能發生水解,電離反應式為HPO42-?PO43-+H+,水解反應式為HPO42-+H2O?H2PO4-+OH-,溶液呈堿性,說明水解程度大于電離程度;由于HPO42-離子和Ca2+離子反應生成沉淀:3Ca2++2HPO42-═Ca3(PO4)2↓+2H+,促進HPO42-的電離,溶液則顯酸性;
故答案為:2.1~7.2;3Ca2++2HPO42-=Ca3(PO4 )2↓+2H+.
(4)Cu元素的化合價由+2價降低到+1價,CuSO4是氧化劑,P4部分磷元素由0價降低到-3價,部分磷元素由0價升高到+5價,磷元素的化合價既升高又降低,所以P4既是氧化劑又是還原劑,若有11molP4參加反應,其中5mol的P4做氧化劑,60mol硫酸銅做氧化劑,只有6mol的P4做還原劑,
則由電子守恒可知,有60mol的CuSO4參加反應,60molCuSO4得到60mol電子,1molP4參加反應失去20mol電子,所以60molCuSO4能氧化白磷的物質的量是$\frac{60}{20}$=3mol,
故答案為:3mol.
點評 本題考查反應熱的計算、PH計算、氧化還原反應電子轉移計算,離子方程式的書寫等知識,側重于學生的分析能力和計算能力的考查,為高考常見題型和高頻考點,題目難度中等.


 期末寶典單元檢測分類復習卷系列答案
期末寶典單元檢測分類復習卷系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 白熾燈工作時,電能全部轉化為光能 | |
| B. | 風力發電時,風能主要轉化為電能 | |
| C. | 煤燃燒時,化學能主要轉化熱能 | |
| D. | 電解水生成H2和O2時,電能主要轉化為化學能 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 該元素原子中共有25個電子 | B. | 該元素原子核外有4個能層 | ||
| C. | 該元素原子最外層共有2個電子 | D. | 該元素原子M電子層共有8個電子 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①④⑤⑧⑨ | B. | ①②③⑥⑦⑨ | C. | ①②③④⑥⑦⑨⑩ | D. | ①②③④⑥⑦⑨ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
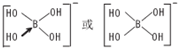 ,
,查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 淀粉、纖維素、蛋白質均屬于天然高分子化合物,水解產物都只有一種 | |
| B. | 油脂在堿性條件下水解屬于皂化反應,酸性條件下的水解產物為甘油和高級脂肪酸 | |
| C. | 用pH計、電導率儀(一種測量溶液導電能力的儀器)均可監測乙酸乙酯的水解程度 | |
| D. | TiCl4+(x+2)H2O$\stackrel{△}{?}$TiO2•xH2O↓+4HCl 屬于水解反應 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com