
| 序號 | 電極1 | 電極2 | 溶液 |
| A | Cu | Cu | 稀H2SO4 |
| B | Ag | Zn | 稀H2SO4 |
| C | Cu | Cu | 酒精 |
| D | C | C | ZnSO4溶液 |
| A. | A | B. | B | C. | C | D. | D |
分析 原電池的構成條件是:①有兩個活潑性不同的電極,②將電極插入電解質溶液中,③兩電極間構成閉合回路,④能自發的進行氧化還原反應;能構成原電池,觀察到有電流產生,據此判斷分析.
解答 解:A.兩個電極為同種金屬,不滿足構成原電池的條件,所以不能構成原電池,故A錯誤;
B.Zn作負極,Ag為正極,正極上氫離子得電子,該裝置符合原電池構成條件,所以能構成原電池,能產生電流,故B正確;
C.酒精屬于非電解質,不滿足構成原電池的條件,所以不能構成原電池,故C錯誤;
D.該裝置不能自發進行氧化還原反應,不滿足構成原電池的條件,所以不能構成原電池,故D錯誤;
故選B.
點評 本題考查了原電池的判斷,題目難度不大,根據原電池的構成條件及工作原理判斷即可,側重于考查對基礎知識的應用能力.


科目:高中化學 來源: 題型:解答題
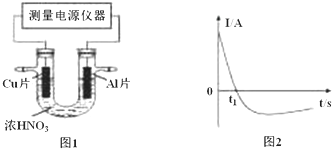
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
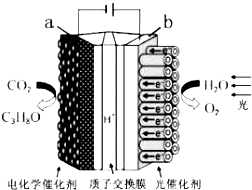 某模擬“人工樹葉”電化學實驗裝置如圖所示,該裝置能將H2O和CO2轉化為O2和燃料(C3H8O).下列說法正確的是( )
某模擬“人工樹葉”電化學實驗裝置如圖所示,該裝置能將H2O和CO2轉化為O2和燃料(C3H8O).下列說法正確的是( )| A. | 該裝置將化學能轉化為光能和電能 | |
| B. | 該裝置工作時,H+從b極區向a極區遷移 | |
| C. | 每生成3mol O2,有44.8LCO2被還原 | |
| D. | a電極的反應為:3CO2+16H+-18e-=C3H8O+4H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
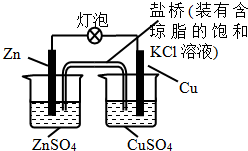
| A. | 一段時間后,銅棒上有紅色物質析出 | |
| B. | 正極反應為:Zn-2e-=Zn2+ | |
| C. | 在外電路中,電流從鋅棒流向銅棒 | |
| D. | 鹽橋中的K+移向ZnSO4溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Cl-的結構示意圖: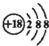 | |
| B. | NaClO的電子式: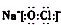 | |
| C. | 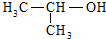 的名稱:2-甲基乙醇 的名稱:2-甲基乙醇 | |
| D. | 質子數為53,中子數為78的碘原子:${\;}_{53}^{78}$ I |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CO在平衡時轉化率為10% | |
| B. | 平衡濃度c(CO2)=c(H2) | |
| C. | 平衡時氣體平均相對分子質量約為23.3 | |
| D. | 其他條件不變時,縮小體積,H2O(g)的轉化率隨之降低 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com