
| A. | 實驗室可用排飽和食鹽水的方法收集氯氣 | |
| B. | 將氯化銅溶液加熱蒸干最終得不到氯化銅固體 | |
| C. | 鋼鐵在潮濕的空氣中容易生銹 | |
| D. | 常溫下,Ksp(MnS)>Ksp(CuS),工業上可用MnS除去廢水中的Cu2+ |
分析 勒夏特列原理為:如果改變影響平衡的條件,平衡將向著能夠減弱這種改變的方向移動;在使用勒夏特列原理時,反應必須是可逆反應且存在平衡移動,否則勒夏特列原理不適用.
解答 解:A、氯氣和水反應生成鹽酸和次氯酸,該反應存在溶解平衡,飽和食鹽水中含有氯化鈉電離出的氯離子,飽和食鹽水抑制了氯氣的溶解,所以實驗室可用排飽和食鹽水的方法收集氯氣,能用勒沙特列原理解釋,故A不選;
B、氯化銅溶液中水解生成氫氧化銅和氯化氫,加熱促進水解,氯化氫揮發得到水解產物氫氧化銅,加熱蒸干最終得不到氯化銅固體,可以用平衡移動原理來解釋,故B不符合;
C、鋼鐵在潮濕的空氣中容易生銹,是鐵的吸氧腐蝕,原電池反應,不能用平衡移動原理來解釋,故C符合;
D、工業上可用MnS除去廢水中的銅離子,平衡向溶度積極小的硫化銅方向轉化,可以用平衡移動原理來解釋,故D不符合;
故選C.
點評 本題考查勒夏特例原理應用的有關判斷,是高考中的常見題型和考點,屬于中等難度試題的考查.試題難易適中,基礎性強,側重對學生解題能力的培養與訓練,旨在考查學生靈活運用基礎知識解決實際問題的能力.該題需要明確的應注意區別化學平衡移動原理和化學反應速率理論的應用范圍,并能具體問題、具體分析加快.


 口算心算速算應用題系列答案
口算心算速算應用題系列答案 同步拓展閱讀系列答案
同步拓展閱讀系列答案科目:高中化學 來源: 題型:選擇題
| A. | N2→NH3→NO→NO2→HNO3 | B. | Na→Na2O2→NaOH→Na2CO3 | ||
| C. | S→SO3→H2SO4→Na2SO4 | D. | Si→SiO2→Na2SiO3→H2SiO3 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 23gNa在氧氣中完全燃燒失電子數為0.5NA | |
| B. | 1mol NO和1mol O2的混合氣體中含有的分子數為2NA | |
| C. | 標準狀況下,11.2L SO3所含分子數為0.5NA | |
| D. | 1.5mol NO2與足量H2O反應,轉移的電子數為NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CH3CH2CH(CH3)2屬于鏈狀化合物 | B. |  屬于芳香化合物 屬于芳香化合物 | ||
| C. |  屬于脂環化合物 屬于脂環化合物 | D. |  屬于芳香化合物 屬于芳香化合物 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CO的燃燒熱為566 kJ/mol | |
| B. | 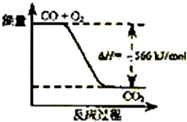 如圖可表示由CO生成CO2的反應過程和能量關系 | |
| C. | 2Na2O2(s)+2CO2(s)═2Na2CO3(s)+O2(g)△H<-452 kJ/mol | |
| D. | CO2(g)與Na2O2(s)反應放出452kJ熱量時,電子轉移數為4NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 如圖是某學校實驗室從化學試劑商店買回的硫酸試劑標簽上的部分內容.據此,下列說法正確的是( )
如圖是某學校實驗室從化學試劑商店買回的硫酸試劑標簽上的部分內容.據此,下列說法正確的是( )| A. | 該硫酸的物質的量濃度為18.4 mol/L | |
| B. | 1 mol Zn與足量的該硫酸反應,產生22.4 L氫氣 | |
| C. | 配制20 mL 4.6 mol/L的稀硫酸需用量筒取該硫酸5.00 mL | |
| D. | 該硫酸與等體積的水混合后所得溶液的物質的量濃度等于9.2 mol/L |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com