
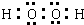 ;[Fe(C2O4)3]3-的名稱是三草酸合鐵(Ⅲ)離子(或三草酸合鐵離子,或三草酸合鐵酸根).
;[Fe(C2O4)3]3-的名稱是三草酸合鐵(Ⅲ)離子(或三草酸合鐵離子,或三草酸合鐵酸根).分析 (1)H2O2為共價化合物,[Fe(C2O4)3]3-為絡離子;
(2)根據原子守恒來配平化學反應方程式;
(3)草酸被H2O2氧化生成水和二氧化碳;
(4)K3[Fe(C2O4)3]•3H2O中的鐵為亞鐵離子,而鐵離子遇KSCN溶液變為血紅色;
(5)A→KCN+Fe3C+C+N2,n(N2)=0.1mol,n(Fe3C)=0.1mol×$\frac{1}{3}$,n(C)=$\frac{0.1mol×\frac{1}{3}×180g/mol×\frac{1}{3}}{12g/mol}$=$\frac{1}{6}$mol,n(KCN)=$\frac{36.8g-0.1mol×28g/mol-6g-2g}{65g/mol}$=0.4mol,確定原子個數比得出化學式.
解答 解:(1)H2O2為共價化合物,其電子式為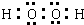 ,[Fe(C2O4)3]3-為絡離子,名稱為三草酸合鐵(Ⅲ)離子(或三草酸合鐵離子,或三草酸合鐵酸根),故答案為:
,[Fe(C2O4)3]3-為絡離子,名稱為三草酸合鐵(Ⅲ)離子(或三草酸合鐵離子,或三草酸合鐵酸根),故答案為: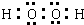 ;[Fe(C2O4)3]3-為絡離子,名稱為三草酸合鐵(Ⅲ)離子(或三草酸合鐵離子,或三草酸合鐵酸根);
;[Fe(C2O4)3]3-為絡離子,名稱為三草酸合鐵(Ⅲ)離子(或三草酸合鐵離子,或三草酸合鐵酸根);
(2)根據水的個數的最小公倍數為6,則FeC2O4•2H2O的化學計量數為2,K3[Fe(C2O4)3]•3H2O的化學計量數為3,然后由原子守恒可知,該化學反應為2FeC2O4•2H2O+H2O2+3K2C2O4+H2C2O4=2K3[Fe(C2O4)3]•3H2O,故答案為:2;1;3;1;2;
(3)草酸被H2O2氧化生成水和二氧化碳,該反應為H2C2O4+H2O2=2CO2↑+2H2O,故答案為:H2C2O4+H2O2=2CO2↑+2H2O;
(4)K3[Fe(C2O4)3]•3H2O中的鐵為亞鐵離子,則不能用KSCN溶液檢驗K3[Fe(C2O4)3]•3H2O中的鐵元素,檢驗鐵元素的方案為取適量晶體加熱,取固體殘留物溶解在H2SO4中,取上層清液于試管中,滴加KSCN溶液.若溶液呈血紅色則有鐵元素,反之則無,
故答案為:否;取適量晶體加熱,取固體殘留物溶解在H2SO4中,取上層清液于試管中,滴加KSCN溶液.若溶液呈血紅色則有鐵元素,反之則無;
(5)由題意可知,A→KCN+Fe3C+C+N2,n(N2)=0.1mol,n(Fe3C)=0.1mol×$\frac{1}{3}$,n(C)=$\frac{0.1mol×\frac{1}{3}×180g/mol×\frac{1}{3}}{12g/mol}$=$\frac{1}{6}$mol,n(KCN)=$\frac{36.8g-0.1mol×28g/mol-6g-2g}{65g/mol}$=0.4mol,則K、Fe、C、N的原子個數比為4:1:6:6,則化學式為K4Fe(CN)6,故答案為:K4Fe(CN)6.
點評 本題考查知識點較多,涉及電子式、反應的配平、氧化還原反應、離子的檢驗及化學式的確定,(5)中注意利用守恒來解答,題目難度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:選擇題
| A. | 1mol氧氣的體積約為22.4L | |
| B. | 標準狀況下,1mol水的體積約為22.4L | |
| C. | 1mol任何氣體,只有在標準狀況下體積才約為22.4L | |
| D. | 同溫同壓下,相同體積的兩種氣體的物質的量一定相等 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 碳-12的原子符號:12 6C | |
| B. | 次氯酸分子的結構式:H-O-Cl | |
| C. | 硫離子的電子排布式為:1s22s22p63s23p6 | |
| D. | 二氧化硅的分子式:SiO2 |
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
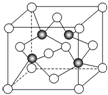 已知A、B、C、D、E、F都是元素周期表中前四周期的元素,它們的核電荷數依次遞增.B原子的P軌道半充滿,形成氫化物的沸點是同主族元素的氫化物中最低的.D原子得到一個電子后3P軌道全充滿.A+比D原子形成的離子少一個電子層.C與A形成A2C型離子化合物.E的原子序數為31,F與B屬同一主族,E與F形成的化合物常用于制造半導體.根據以上信息,回答下列問題:
已知A、B、C、D、E、F都是元素周期表中前四周期的元素,它們的核電荷數依次遞增.B原子的P軌道半充滿,形成氫化物的沸點是同主族元素的氫化物中最低的.D原子得到一個電子后3P軌道全充滿.A+比D原子形成的離子少一個電子層.C與A形成A2C型離子化合物.E的原子序數為31,F與B屬同一主族,E與F形成的化合物常用于制造半導體.根據以上信息,回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
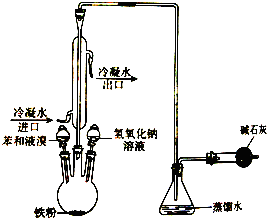 如圖是實驗室制取溴苯的裝置圖,請回答下列問題:
如圖是實驗室制取溴苯的裝置圖,請回答下列問題:
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
 ,該化合物屬于離子化合物(填“共價”或“離子”).
,該化合物屬于離子化合物(填“共價”或“離子”). ,該化合物含的化學鍵類型是共價鍵.
,該化合物含的化學鍵類型是共價鍵.查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 由 CH3CH2OH(l)+3O2(g)═2CO2(g)+3H2O(g)△H=-1366.8 kJ•mol-1,可知乙醇的標準燃燒熱為1366.8 kJ•mol-1 | |
| B. | 已知:C(金剛石,s)=C(石墨,s)△H<0,則金剛石比石墨穩定 | |
| C. | 已知:N2(g)+O2(g)═2NO(g)△H=+180 kJ•mol-1 2CO(g)+O2(g)═2CO2 (g)△H=-566 kJ•mol-1 則 2CO(g)+2NO(g)═N2 (g)+2CO2(g)△H=-746 kJ•mol-1 | |
| D. | OH-(aq)+H+(aq)═H2O(l)△H=-57.3 kJ•mol-1 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com