
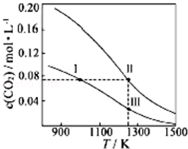
| A. | 體系中c(CO):c(CO,狀態Ⅱ)<2c(CO,狀態Ⅲ) | |
| B. | 反應CO2(g)+C(s)?2CO(g)的△S>0、△H<0 | |
| C. | 體系的總壓強P總:P總(狀態Ⅱ)<2P總(狀態Ⅰ) | |
| D. | 逆反應速率V逆:V逆(狀態Ⅰ)>V逆(狀態Ⅲ) |
分析 A.狀態II、狀態Ⅲ的溫度相同,狀態II看作先加入0.1molCO2,與狀態Ⅲ平衡時CO的濃度相同,再加入0.1molCO2,若平衡不移動,Ⅱ狀態CO的濃度等于2倍Ⅲ,但再充入CO2,相當增大壓強,平衡左移動,消耗CO;
B.由氣體的化學計量數增大可知△S,由圖中溫度高平衡時c(CO2)小可知△H;
C.分別加入0.1molCO2和0.2molCO2,曲線I為加入0.1molCO2,曲線II為加入0.2molCO2,加壓CO2(g)+C(s)?2CO(g)平衡逆向移動;
D.狀態I、狀態Ⅲ的溫度不同,溫度高反應速率快.
解答 解:A.狀態II、狀態Ⅲ的溫度相同,狀態II看作先加入0.1molCO2,與狀態Ⅲ平衡時CO的濃度相同,再加入0.1molCO2,若平衡不移動,Ⅱ狀態CO的濃度等于2倍Ⅲ,但再充入CO2,相當增大壓強,平衡左移,消耗CO,則c(CO,狀態Ⅱ)<2c(CO,狀態Ⅲ),故A正確
B.由氣體的化學計量數增大可知△S>0,由圖中溫度高平衡時c(CO2)小,則升高溫度平衡正向移動,可知△H>0,故B錯誤;
C.分別加入0.1molCO2和0.2molCO2,曲線I為加入0.1molCO2,曲線II為加入0.2molCO2,若平衡不移動,體系的總壓強為P總(狀態Ⅱ)=2P總(狀態Ⅰ),但加壓CO2(g)+C(s)?2CO(g)平衡逆向移動,為使c(CO2)相同,則加熱使平衡正向移動,則體系的總壓強為P總(狀態Ⅱ)>2P總(狀態Ⅰ),故C錯誤;
D.狀態I、狀態Ⅲ的溫度不同,溫度高反應速率快,則逆反應速率為V逆(狀態Ⅰ)<V逆(狀態Ⅲ),故D錯誤;
故選A.
點評 本題考查化學平衡及平衡的建立,為高頻考點,把握平衡移動的影響因素、圖象分析為解答的關鍵,選項BC為解答的難點,題目難度中等.


 口算題天天練系列答案
口算題天天練系列答案科目:高中化學 來源: 題型:選擇題
| A. | 0.1mol•L-1MgCl2溶液 | B. | 0.1mol•L-1NH4Cl溶液 | ||
| C. | 0.1mol•L-1KCl溶液 | D. | 0.1mol•L-1 AlCl3溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
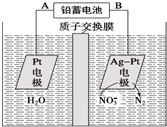
| A. | 鉛蓄電池的A極為正極,電極材料為PbO2 | |
| B. | 該電解池的總反應方程式為:2H2O+4NO3- $\frac{\underline{\;電解\;}}{\;}$2N2↑+5O2↑+4OH- | |
| C. | 該電解池的陰極反應式為:2NO3-+12H++10e-═N2↑+6H2O | |
| D. | 若電解過程中轉移2mol電子,則交換膜右側電解液的質量減少5.6g |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
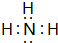 ,BA3跟C的單質在一定條件下反應,能生成化合物BC的化學方程式4NH3+5O2$\frac{\underline{催化劑}}{△}$4NO+6H2O.
,BA3跟C的單質在一定條件下反應,能生成化合物BC的化學方程式4NH3+5O2$\frac{\underline{催化劑}}{△}$4NO+6H2O.查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 它們的原子序數B>A>C | B. | 它們的離子半徑A2->C->B2+ | ||
| C. | 它們的原子半徑C>B>A | D. | 它們的最外層電子數C>A>B |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 23g Na在空氣中完全燃燒,轉移的電子數為1 mol | |
| B. | 78gNa2O2含有的離子數為3NA | |
| C. | 0.1 mol Fe與足量水蒸氣反應生成H2的分子數為0.1NA | |
| D. | 5.4 g鋁與足量NaOH溶液反應,產生6.72L的氫氣 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在NaHS溶液中滴入少量CuCl2溶液,產生黑色沉淀,HS-水解程度增大 | |
| B. | 100℃時,將pH=2的鹽酸與pH=12的NaOH溶液等體積混合,溶液顯中性 | |
| C. | 0.1 mol•L-1 Na2SO3溶液加入少量NaOH固體,c(SO32-)與c(Na+)均增大 | |
| D. | 常溫下pH=7的NaHSO3與Na2SO3混合溶液中:c(Na+)=c(HSO3-)+c(SO32-) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com