
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 一 | ① | |||||||
| 二 | ② | ③ | ④ | |||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
 ;⑦元素為硅;⑨元素的離子為Cl-,最外層電子式為8,帶一個單位負電荷,其電子式為:
;⑦元素為硅;⑨元素的離子為Cl-,最外層電子式為8,帶一個單位負電荷,其電子式為: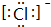 ,故答案為:
,故答案為: ;硅;
;硅;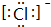 ;
; ;⑤與⑧形成化合物為Na2S,由鈉離子與硫離子構成,用Na原子、S原子電子式表示其形成為:
;⑤與⑧形成化合物為Na2S,由鈉離子與硫離子構成,用Na原子、S原子電子式表示其形成為: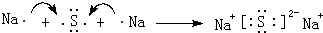 ,
, ;
;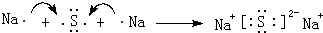 ;
;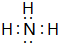 ;N原子、H原子的電負性不同,對鍵合電子吸引能力不同,故二者之間形成極性鍵;氨氣溶于水生成一水合氨,一水合氨電離出銨根離子與氫氧根離子,溶液呈堿性,
;N原子、H原子的電負性不同,對鍵合電子吸引能力不同,故二者之間形成極性鍵;氨氣溶于水生成一水合氨,一水合氨電離出銨根離子與氫氧根離子,溶液呈堿性,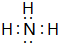 ;極性鍵;堿;
;極性鍵;堿;

科目:高中化學 來源: 題型:
| A、①②③⑤ | B、②④⑤⑥ |
| C、①②④⑤ | D、②③④⑥ |
查看答案和解析>>
科目:高中化學 來源: 題型:
| 族 周期 | IA | 0 | ||||||
| 一 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 二 | ② | ③ | ④ | |||||
| 三 | ⑤ | ⑨ | ⑥ | ⑦ | ⑧ | |||
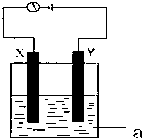
 X溶液與Y溶液反應的離子方程式為
X溶液與Y溶液反應的離子方程式為查看答案和解析>>
科目:高中化學 來源: 題型:
 下圖是元素周期表短周期中11種元素的化臺價與原子序數的關系示意圖,請回答下列問題(用具體的元素符號作答):
下圖是元素周期表短周期中11種元素的化臺價與原子序數的關系示意圖,請回答下列問題(用具體的元素符號作答):查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
 1、欲用98%的濃硫酸(ρ=1.84g?cm-3)配制成濃度為0.25mol?L-1的稀硫酸500mL.
1、欲用98%的濃硫酸(ρ=1.84g?cm-3)配制成濃度為0.25mol?L-1的稀硫酸500mL.| a | b | c | d | e | |
| 砝碼大小/g | 100 | 50 | 20 | 10 | 5 |
查看答案和解析>>
科目:高中化學 來源: 題型:
 A、B、C均為短周期元素,它們在周期表中的位置如圖所示:B、C原子最外層電子數之和等于A原子最外層電子數的2倍;B、C元素的原子序數之和是A元素的原子序數的4倍.則元素符號:A是
A、B、C均為短周期元素,它們在周期表中的位置如圖所示:B、C原子最外層電子數之和等于A原子最外層電子數的2倍;B、C元素的原子序數之和是A元素的原子序數的4倍.則元素符號:A是查看答案和解析>>
科目:高中化學 來源: 題型:
 (1)實事證明,能設計成原電池的反應通常是放熱反應,下列化學反應在理論上可以設計成原電池的是
(1)實事證明,能設計成原電池的反應通常是放熱反應,下列化學反應在理論上可以設計成原電池的是查看答案和解析>>
科目:高中化學 來源: 題型:
| A、隨原子序數的遞增,元素原子的核外電子數增多,原子半徑逐漸減小 |
| B、若兩種不同的核素具有相同的中子數,則二者一定不屬于同種元素 |
| C、Si、P、S、Cl 相應的氧化物對應水化物的酸性依次增強 |
| D、在元素周期表中,各主族元素的最高化合價與其族序數相等 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com