
| A. | 硫化亞鐵和稀鹽酸反應:FeS+2H+=Fe2++H2S↑ | |
| B. | 次氯酸鈉溶液中通入少量SO2反應:SO2+H2O+ClO-=SO42-+Cl-+2H+ | |
| C. | 過氧化鈉加入足量稀硫酸反應:2Na2O2+4H+═4Na++O2↑+2H2O | |
| D. | 銅粉中加入溴化鐵溶液反應:2Fe3++Cu=2Fe2++Cu2+ |
分析 A.硫化亞鐵和稀鹽酸反應生成硫酸亞鐵和硫化氫;
B.次氯酸鈉具有強氧化性,能氧化二氧化硫生成硫酸根離子,自身被還原生成氯離子,因二氧化硫少量,所以有次氯酸生成;
C.過氧化鈉與足量稀硫酸反應生成硫酸鈉、氧氣和水;
D.銅和溴化鐵反應,生成溴化亞鐵、溴化銅.
解答 解:A.硫化亞鐵難溶于水,硫化氫為氣體,兩者在離子反應方程式中寫化學式,所以硫化亞鐵與稀硫酸反應的離子反應為FeS+2H+=Fe2++H2S↑,故A正確;
B.次氯酸鈉具有強氧化性,能氧化二氧化硫生成硫酸根離子,自身被還原生成氯離子,因二氧化硫少量,所以有次氯酸生成,離子方程式為3ClO-+SO2+H2O=Cl-+SO42-+2HClO,故B錯誤;
C.過氧化鈉、氧氣、水在離子反應方程式中寫化學式,所以過氧化鈉加入足量稀硫酸反應,離子方程式為:2Na2O2+4H+═4Na++O2↑+2H2O,故C正確;
D.鐵離子具有氧化性,銅粉中加入溴化鐵溶液,離子方程式為:2Fe3++Cu=2Fe2++Cu2+,故D正確;
故選B.
點評 本題考查離子反應的書寫,明確發生的化學反應是解答本題的關鍵,注意離子反應的書寫方法及離子反應中保留化學式的物質,題目難度不大.


科目:高中化學 來源: 題型:選擇題
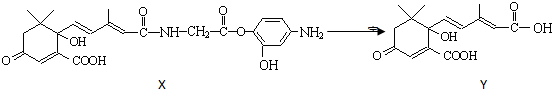 ( )
( )| A. | Y既可以與FeCl3溶液發生顯色反應,又可使酸性KMnO4溶液褪色 | |
| B. | 1 molY與足量NaOH溶液反應,最多消耗3 mol NaOH | |
| C. | 1 molX最多能加成9 molH2 | |
| D. | X可以發生氧化、取代、酯化、加聚、縮聚反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
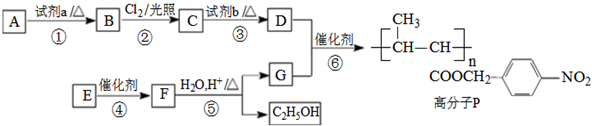
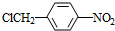 .
.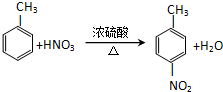 .
.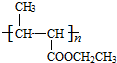 +nH2O$→_{△}^{H+}$
+nH2O$→_{△}^{H+}$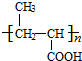 +n CH3CH2OH.
+n CH3CH2OH.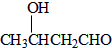 以乙烯為起始原料,選用必要的無機試劑合成E,寫出合成路線(用結構簡式表示有機物,用箭頭表示轉化關系,箭頭上注明試劑和反應條件).
以乙烯為起始原料,選用必要的無機試劑合成E,寫出合成路線(用結構簡式表示有機物,用箭頭表示轉化關系,箭頭上注明試劑和反應條件).查看答案和解析>>
科目:高中化學 來源: 題型:解答題
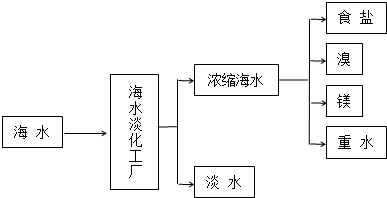
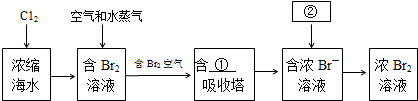
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | K+、CO32-、S2-、Cl- | B. | NO3-、Br-、Na+、NH4+ | ||
| C. | Na+、K+、Cl-、HS- | D. | Na+、NO3-、Fe3+、SO4- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 過氧化鈉與水反應時,生成0.1molO2轉移的電子數為0.2NA | |
| B. | 4.48L氨氣分子中含0.6NA個N-H鍵 | |
| C. | 100ml0.2mol•L-1的FeCl3溶液中,含Fe3+數為0.02NA | |
| D. | 密閉容器中2molNO與1molO2充分反映,產物的分子數為2NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1molFe溶于硝酸,電子轉移數為3NA | |
| B. | 12.0gNaHSO4固體中含陽離子數為0.1NA | |
| C. | 標準狀態下,22.4L氟化氫中含有氟原子數為NA | |
| D. | 7.8gNa2O2與足量的水反應轉移電子數為0.2NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 元素 | 甲 | 乙 | 丙 | 丁 |
| 原子半徑/nm | 0.186 | 0.102 | 0.152 | 0.074 |
| 主要化合價 | +1 | +6、-2 | +1 | -2 |
| A. | 甲的最高價氧化物對應水化物的堿性比丙的強 | |
| B. | 甲單質可用電解其鹽溶液的方法冶煉而得 | |
| C. | 常溫下,丁的兩種氫化物均為液體 | |
| D. | 乙的簡單離子是四種元素各自形成的簡單離子中半徑最大的 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com