
| A. | 使酚酞變紅色的溶液中:Na+、Al3+、SO42-、Cl- | |
| B. | 水電離的c(H+)=1×10-13mol•L-1的溶液中:K+、Na+、AlO2-、CO32- | |
| C. | $\frac{{k}_{w}}{c({H}^{+})}$=1×10-13mol•L-1的溶液中:NH4+、Ba2+、Cl-、NO3- | |
| D. | 與Al反應能放出H2的溶液中:Fe2+、K+、NO3-、SO42- |
分析 A.使酚酞變紅色的溶液呈堿性;
B.水電離的c(H+)=1×10-13mol•L-1的溶液可能呈酸性或堿性;
C.$\frac{{k}_{w}}{c({H}^{+})}$=1×10-13mol•L-1的溶液呈酸性;
D.與Al反應能放出H2的溶液可能為強堿性或非氧化性酸溶液.
解答 解:A.使酚酞變紅色的溶液呈堿性,堿性條件下Al3+不能大量共存,故A錯誤;
B.水電離的c(H+)=1×10-13mol•L-1的溶液可能呈酸性或堿性,酸性條件下AlO2-、CO32-不能大量存在,故B錯誤;
C.$\frac{{k}_{w}}{c({H}^{+})}$=1×10-13mol•L-1的溶液呈酸性,酸性條件下離子之間不發(fā)生任何反應,可大量共存,故C正確;
D.與Al反應能放出H2的溶液可能為強堿性或非氧化性酸溶液,酸性條件下Fe2+、NO3-發(fā)生氧化還原反應不能大量共存,堿性條件下Fe2+不能大量共存,故D錯誤.
故選C.
點評 本題考查離子共存,側重考查復分解反應、氧化還原反應,為高考高頻點,明確離子共存條件及離子性質(zhì)即可解答,易錯選項是D.


科目:高中化學 來源: 題型:填空題
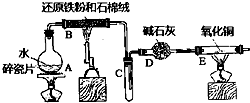 某校化學小組學生利用如圖所列裝置進行“鐵與水反應”的實驗,并進行了其他有關實驗.(圖中夾持及尾氣處理裝置均已略去)
某校化學小組學生利用如圖所列裝置進行“鐵與水反應”的實驗,并進行了其他有關實驗.(圖中夾持及尾氣處理裝置均已略去)查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
| A. | 0~6min的平均反應速率:v(H2O2)≈3.3×10-2mol/(L•min) | |
| B. | 6~10min的平均反應速率:v(H2O2)<3.3×10-2mol/(L•min) | |
| C. | 反應至6min時,c(H2O2)=0.3mol/L | |
| D. | 反應至6min時,H2O2分解了50% |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 萃取操作時,應選擇有機萃取劑,且萃取劑的密度必須比水大 | |
| B. | 用蒸發(fā)的方法使NaCl從溶液中析出時,玻璃棒的作用是引流 | |
| C. | 蒸餾操作時,應使溫度計水銀球插入蒸餾燒瓶的液面以下 | |
| D. | 分液時,分液漏斗下層液體從下口放出,上層液體從上口倒出 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 使用催化劑能加快反應速率 | |
| B. | 壓強增大不影響化學反應速率 | |
| C. | 冬天氣溫低,反應速率降低,對人類危害減小 | |
| D. | 無論外界條件怎樣改變,均對此化學反應的速率無影響 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鈉在氯氣中燃燒 | B. | 二氧化碳通入澄清的石灰水中 | ||
| C. | 氯化鈉溶液中滴加硝酸銀溶液 | D. | 鋅粒放入稀硫酸中 |
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
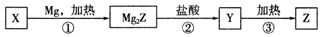
| A. | X可以和氫氟酸反應 | |
| B. | 甲烷的穩(wěn)定性比Y強 | |
| C. | Z是將太陽能轉換為電能的常用材料 | |
| D. | 上述①②③變化過程中,依次發(fā)生置換反應、復分解反應和分解反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在化學反應中,化學能只可以轉化為熱能 | |
| B. | 化學鍵的斷裂和形成是化學反應中能量變化的主要原因 | |
| C. | 已知2H2(g)+O2(g)=2H2O(l)△H<0,當反應達平衡后升高溫度,反應逆向移動,逆反應速率增大,正反應速率減小 | |
| D. | 合成氨反應N2+3H2?2NH3,當N2、H2、NH3濃度相等時該反應達到了最大限度 |
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com