
某溶液只可能含有以下離子中的若干種:H+、NH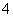 、K+、Mg2+、NO
、K+、Mg2+、NO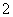 、CO
、CO 、NO
、NO ,現取兩份200 mL溶液進行如下實驗:(已知HNO2不穩定極易分解2HNO2===H2O+NO2↑+NO↑)
,現取兩份200 mL溶液進行如下實驗:(已知HNO2不穩定極易分解2HNO2===H2O+NO2↑+NO↑)
①第一份加足量AgNO3溶液后,有11.68 g白色沉淀產生,沉淀中加入足量稀鹽酸充分反應,有棕色氣體產生,沉淀顏色不變,但是質量減少0.2 g;②將產生的氣體全部通入過量的澄清石灰水,又得到白色沉淀2.0 g,該沉淀能溶于稀鹽酸產生無色氣體;③第二份加入過量濃NaOH溶液,加熱使產生的氣體全部放出,用100 mL 0.5 mol·L-1的稀硫酸恰好完全吸收,酸也不剩余。
根據上述實驗,以下推測不正確的是( )
A.原溶液一定不存在較大濃度的H+、Mg2+
B.原溶液確定含NH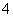 、NO
、NO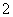 、CO
、CO ,且物質的量之比為5:2:1
,且物質的量之比為5:2:1
C.不能確定原溶液是否含有K+、NO
D.實驗中產生的棕色氣體遇空氣顏色會加深
解析:本題考查了離子檢驗,意在考查考生的計算能力和判斷能力。根據實驗①②可推知,溶液中含有CO 、NO
、NO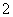 ,則一定不存在較大濃度的H+、Mg2+,A選項正確;根據實驗③可知含有NH
,則一定不存在較大濃度的H+、Mg2+,A選項正確;根據實驗③可知含有NH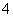 ,由H2SO4+2NH3===(NH4)2SO4得,n(NH
,由H2SO4+2NH3===(NH4)2SO4得,n(NH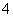 )=2n(SO
)=2n(SO )=2×0.1 L×0.5 mol·L-1=0.1 mol;11.68 g沉淀為Ag2CO3和AgNO2的混合物,n(CO
)=2×0.1 L×0.5 mol·L-1=0.1 mol;11.68 g沉淀為Ag2CO3和AgNO2的混合物,n(CO )=n(CaCO3)=2.0 g÷100 g·mol-1=0.02 mol,則m(Ag2CO3)=0.02 mol×276 g·mol-1=5.52 g,m(AgNO2)=11.68 g-5.52 g=6.16 g,n(NO
)=n(CaCO3)=2.0 g÷100 g·mol-1=0.02 mol,則m(Ag2CO3)=0.02 mol×276 g·mol-1=5.52 g,m(AgNO2)=11.68 g-5.52 g=6.16 g,n(NO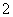 )=n(AgNO2)=6.16 g÷154 g·mol-1=0.04 mol,所以原溶液確定含NH
)=n(AgNO2)=6.16 g÷154 g·mol-1=0.04 mol,所以原溶液確定含NH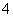 、NO
、NO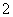 、CO
、CO ,且物質的量之比為5:2:1,B選項正確;根據電荷守恒可知,溶液中一定有NO
,且物質的量之比為5:2:1,B選項正確;根據電荷守恒可知,溶液中一定有NO ,不能確定是否含有K+,C選項錯誤;產生的棕色氣體為NO、NO2和CO2的混合物,NO遇空氣會生成NO2,顏色會加深,D選項正確。
,不能確定是否含有K+,C選項錯誤;產生的棕色氣體為NO、NO2和CO2的混合物,NO遇空氣會生成NO2,顏色會加深,D選項正確。
答案:C


科目:高中化學 來源: 題型:
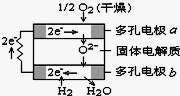
固體氧化物燃料電池是由美國西屋(Westinghouse)公司研制開發的.它以固體氧化鋯-氧化釔為電解質,這種固體電解質在高溫下允許氧離子(O2-)在其間通過.該電池的工作原理如圖所示,其中多孔電極a、b均不參與電極反應.下列判斷正確的是
A.有O2放電的a極為電池的負極
B.a極對應的電極反應為:O2+ 2H2O+ 4e--= 4OH-
C.有H2放電的一極電極反應為:H2+O2- -2 e- =H2O
D.該電池的總反應方程式為:2H2+ O2= 2H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
常溫下0.1 mol·L-1氨水的pH=a,下列能使溶液pH=(a+1)的措施是
A.加入適量的氫氧化鈉固體 B.將溶液稀釋到原體積的 10倍
C.加入等體積0.2 mol·L-1氨水 D.降低溶液的溫度
查看答案和解析>>
科目:高中化學 來源: 題型:
向某無色溶液中分別進行下列操作,所得現象和結論正確的是( )
A.加入氨水,產生白色沉淀,證明原溶液中存在Al3+
B.加入AgNO3溶液,產生白色沉淀,證明原溶液中存在Cl-
C.加入鹽酸酸化的BaCl2溶液,生成白色沉淀,證明原溶液中存在SO
D.加入NaOH溶液并加熱,產生使濕潤的紅色石蕊試紙變藍的氣體,證明原溶液中存在NH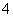
查看答案和解析>>
科目:高中化學 來源: 題型:
某礦樣用過量酸溶解并過濾,所得濾液A主要含CO 、Ni2+、SO
、Ni2+、SO 、H+、Fe2+、Fe3+、OH-、Mg2+、Mn2+等九種離子中的七種。將A中金屬元素進行分離以備利用,部分流程如圖所示:
、H+、Fe2+、Fe3+、OH-、Mg2+、Mn2+等九種離子中的七種。將A中金屬元素進行分離以備利用,部分流程如圖所示:

可能用到的有關數據如下:
| 物質 | 開始沉淀的pH | 沉淀完全的pH | Ksp(25 ℃) |
| Fe(OH)3 | 2.7 | 3.7 | 4.0×10-38 |
| Fe(OH)2 | 7.6 | 9.6 | 8.0×10-16 |
| Ni(OH)2 | 7.2 | 9.2 | 5.5×10-16 |
| Mg(OH)2 | 9.6 | 11.1 | 1.2×10-11 |
請根據題給信息填空:
(1)濾液A中不能大量存在的兩種離子是________。
(2)已知“濾渣1”是MnO2,步驟①發生的氧化還原反應的離子方程式為________。
(3)常溫下,某Ni(OH)2、Mg(OH)2共沉淀的混合體系中,若c(Ni2+)=5.5×10-11 mol·L-1,則c(Mg2+)=________。
(4)假定步驟①中NaClO恰好反應,欲檢驗濾液3中的酸根離子,需優先檢驗________(填離子符號)。
(5)為測定該礦樣中鐵元素的含量,取20.0 g礦石,按上述流程操作,將________(填“濾渣1”、“濾渣2”或“濾渣3”)完全酸溶,再使其中的鐵元素還原為Fe2+,然后將所得溶液稀釋到100 mL,取出20.00 mL用0.100 0 mol·L-1 KMnO4溶液滴定。達到滴定終點時溶液顏色為________色,共消耗KMnO4溶液16. 00 mL,經計算礦樣中鐵元素的質量分數為________。
查看答案和解析>>
科目:高中化學 來源: 題型:
向含有Fe2+、I-、Br-的溶液中通入適量氯氣,溶液中各種離子的物質的量變化如圖所示。有關說法不正確的是( )
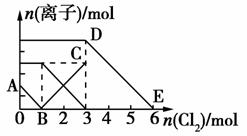
A.線段BC代表Fe3+物質的量的變化情況
B.原混合溶液中n(FeBr2)=3 mol
C.當通入2 mol Cl2時,溶液中已發生的離子反應可表示為:2Fe2++2I-+2Cl2===2Fe3++I2+4Cl-
D.原溶液中n(Fe2+):n(I-):n(Br-)=3:1:2
查看答案和解析>>
科目:高中化學 來源: 題型:
將含O2和CH4的混合氣體充入裝有23.4gNa2O2的密閉容器中,點火花點燃,反應結束后,容器溫度為150℃、壓強為0 Pa。將殘留物溶于水,無氣體逸出。下列敘述正確的是( )
A.原混合氣體中O2和CH4的體積比為2∶1;
B.原混合氣體中O2和CH4的體積比為1∶2;
C.殘留固體中有Na2CO3和NaOH;
D.殘留固體中只有Na2CO3
查看答案和解析>>
科目:高中化學 來源: 題型:
臭氧是理想的煙氣脫硝劑,其脫硝反應為:2NO2(g)+O3(g)  N2O5(g)+O2(g),反應在恒容密閉容器中進行,下列由該反應相關圖像作出的
N2O5(g)+O2(g),反應在恒容密閉容器中進行,下列由該反應相關圖像作出的 判斷正確的是
判斷正確的是
| A | B | C | D |
|
|
|
|
|
| 升高溫度,平衡常數減小 | 0~3s內,反應速率為: v(NO | t1時僅加入催化劑,平衡正向移動 | 達平衡時,僅改變x,則x為c(O2) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com