
分析 (1)①鹽酸是一元強酸完全電離,硫酸是二元強酸完全電離,醋酸是弱酸部分電離;
②鹽酸是一元強酸完全電離,硫酸是二元強酸完全電離,醋酸是弱酸部分電離,c(H+)相同時,醋酸濃度最大;
(2)酸性溶液中水電離出的氫離子濃度等于溶液中氫氧根離子濃度,依據KW=c(H+)×c(OH-)計算;
(3)在一元強堿MOH溶液中加入一元酸HA溶液,充分反應后,溶液呈中性,則有c(OH-)=c(H+),結合電荷守恒分析;
(4)明礬溶于水電離出的鋁離子發生水解反應,生成氫氧化鋁膠體,氫氧化鋁膠體可以吸附雜質,起到凈水作用;
(5)FeCl3是強酸弱堿鹽,鐵離子是弱堿陽離子,將FeCl3溶液蒸干時,鐵離子水解生成Fe(OH)3和HCl,升高溫度促進HCl揮發,所以蒸干溶液時得到堿,灼燒Fe(OH)3時,Fe(OH)3會分解生成氧化鐵.
解答 解:(1)①鹽酸是一元強酸完全電離,氫離子濃度等于酸的濃度;硫酸是二元強酸完全電離,硫酸中氫離子濃度為酸的二倍;醋酸是弱酸部分電離,氫離子的濃度小于酸的濃度;所以c(H+)由大到小的順序是b>a>c,
故答案為:b>a>c;
②鹽酸是一元強酸完全電離,硫酸是二元強酸完全電離,c(H+)相同時,鹽酸物質的量濃度是硫酸的2倍,醋酸是弱酸部分電離,c(H+)相同時,醋酸濃度最大,硫酸的濃度最小,所以物質的量濃度由大到小的順序是c>a>b(或c>a=2b),
故答案為:c>a>b(或c>a=2b);
(2)常溫下,0.1mol/L的HCl溶液中,C(H+)=10-1mol/L,水電離出的氫離子和氫氧根離子濃度相等,溶液中的氫離子全部是水電離出來的,所以水電離出的C(H+)=c(OH-)=$\frac{{1}^{-14}}{0.1}$mol/l=1×10-13mol/L,
故答案為:1×10-13;
(3)混合溶液呈中性,則c(OH-)=c(H+),根據電荷守恒得c(A-)+c(OH-)=c(H+)+c(M+),則c(A-)=c(M+),故甲正確,
故答案為:甲;電荷守恒原理;
(4)明礬[KAl(SO4)2•12H2O]作為凈水劑是因為明礬溶于水電離出的鋁離子發生水解反應,生成氫氧化鋁膠體,氫氧化鋁膠體可以吸附雜質,反應的離子方程式為:Al3++3H2O?Al(OH)3(膠體)+3H+;
故答案為:Al3++3H2O?Al(OH)3(膠體)+3H+;
(5)FeCl3是強酸弱堿鹽,鐵離子是弱堿陽離子.將FeCl3溶液蒸干時,鐵離子水解生成Fe(OH)3和HCl,升高溫度促進HCl揮發,所以蒸干溶液時得到堿,灼燒氫氧化鐵時,氫氧化鐵會分解,反應方程式為2Fe(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Fe2O3+3H2O,所以最終得到的是紅棕色固體Fe2O3,
故答案為:Fe2O3.
點評 本題考查了弱電解質的電離、鹽類的水解應用等知識,題目難度中等,明確鹽的水解原理以及弱電解質電離特點是解本題關鍵,試題知識點較多、綜合性較強,充分考查了學生的靈活應用能力.


科目:高中化學 來源: 題型:填空題
 實驗室里要配制465mL 0.2mol/L的硫酸鈉溶液.
實驗室里要配制465mL 0.2mol/L的硫酸鈉溶液.查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
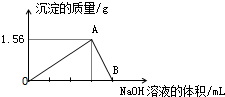 向40mL某AlCl3溶液中滴加2mol•L-1的NaOH溶液時,得到Al(OH)3沉淀的質量與所滴加NaOH溶液的體積(mL)關系如圖所示,試回答下列問題:
向40mL某AlCl3溶液中滴加2mol•L-1的NaOH溶液時,得到Al(OH)3沉淀的質量與所滴加NaOH溶液的體積(mL)關系如圖所示,試回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1molH2O含有的H2O分子數為NA | |
| B. | 1mol金屬鎂與足量的鹽酸完全反應,轉移的電子數為2NA | |
| C. | 11.2L氧氣含有的O2分子數為0.5NA | |
| D. | 將含1molFeCl3的溶液與沸水完全反應,生成的Fe(OH)3膠體粒子數為NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 實驗序號 | 甲 | 乙 | 丙 |
| 合金質量/mg | 255 | 385 | 459 |
| 生成氣體體積/mL | 280 | 336 | 336 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向FeCl3和CuCl2混合溶液中加入鐵粉,有紅色固體析出,氧化性:Cu2+>Fe3+ | |
| B. | 用石墨作電極電解MgSO4溶液,某電極附近有白色沉淀生成該電極為陽極 | |
| C. | 測定中和反應的反應熱時,將堿緩慢倒入酸中,所測結果偏低 | |
| D. | 向某溶液中先滴加硝酸酸化,再滴加BaCl2溶液,有白色沉淀生成 該溶液中一定含有Ag+ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com