
| A. | Na2O2+2H2O═2Na++2OH-+H2↑ | B. | 2O22-+4H+═4OH-+O2↑ | ||
| C. | Na2O2+2H2O═2Na++2OH-+O2↑ | D. | 2Na2O2+2H2O═4Na++4OH-+O2↑ |
 導學教程高中新課標系列答案
導學教程高中新課標系列答案 小學課時特訓系列答案
小學課時特訓系列答案科目:高中化學 來源: 題型:解答題
 太陽能電池是通過光電效應或者光化學效應直接把光能轉化成電能的裝置.其材料除單晶硅,還有銅銦鎵硒等化合物.
太陽能電池是通過光電效應或者光化學效應直接把光能轉化成電能的裝置.其材料除單晶硅,還有銅銦鎵硒等化合物.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CaO+H2O═Ca(OH)2 | B. | 2KClO3$\frac{\underline{\;\;△\;\;}}{\;}$2KCl+3O2↑ | ||
| C. | 2NaOH+CO2═Na2CO3+H2O | D. | Fe+2HCl═H2↑+FeCl2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
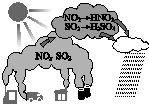
| A. | 汽車尾氣是導致酸雨的原因之一 | B. | 酸雨會使土壤、湖泊酸化 | ||
| C. | 酸雨形成中不涉及氧化還原反應 | D. | 燃煤中加入石灰石可防治酸雨 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 實驗裝置 | 編號 | 溶液X | 實驗現象 |
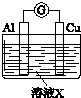 | 實驗Ⅰ | 6mol•L-1稀硝酸 | 電流計指針向右偏轉,銅片表面產生無色氣體,在液面上方變為紅棕色. |
| 實驗Ⅱ | 15mol•L-1濃硝酸 | 電流計指針先向右偏轉,很快又偏向左邊,鋁片和銅片表面產生紅棕色氣體,溶液變為綠色. |
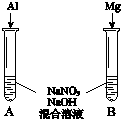 (3)用如圖裝置進行實驗Ⅲ:溶液X為1mol•L-1稀硝酸溶液,觀察到電流計指針向右偏轉.
(3)用如圖裝置進行實驗Ⅲ:溶液X為1mol•L-1稀硝酸溶液,觀察到電流計指針向右偏轉.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
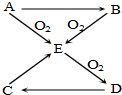 已知A、B、C、D、E五種物質有如圖所示的轉化關系(部分反應物及反應條件未列出,若解題時需要,可作合理假設),且五種物質中均含有A元素.
已知A、B、C、D、E五種物質有如圖所示的轉化關系(部分反應物及反應條件未列出,若解題時需要,可作合理假設),且五種物質中均含有A元素.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
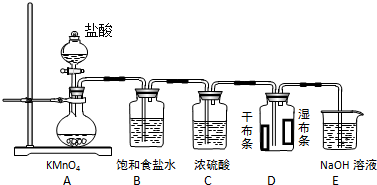
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 實驗序號 | 實驗操作 | 實驗現象 |
| 實驗1 | 向2mL 0.001mol/L NaHCO3溶液中加入1mL 0.1mol/LCaCl2溶液 | 無明顯變化.用激光筆照射,沒有出現光亮的通路. |
| 實驗2 | 向2mL 0.1mol/L NaHCO3溶液中加入1mL 0.1mol/LCaCl2溶液 | 略顯白色均勻的渾濁,用激光筆照射,出現光亮的通路. |
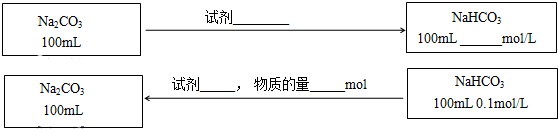
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
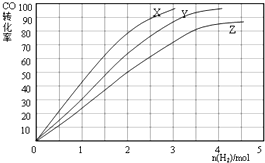
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com