
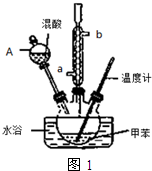
 常見的一硝基甲苯有對硝基甲苯和鄰硝基甲苯兩種,均可用于合成各種染料.某探究小組利用下列反應和裝置制備一硝基甲苯.
常見的一硝基甲苯有對硝基甲苯和鄰硝基甲苯兩種,均可用于合成各種染料.某探究小組利用下列反應和裝置制備一硝基甲苯.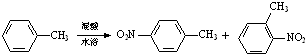
| 密度/g?cm-3 | 沸點/℃ | 溶解性 | |
| 甲苯 | 0.866 | 110.6 | 不溶于水,易溶于硝基甲苯 |
| 對硝基甲苯 | 1.286 | 237.7 | 不溶于水,易溶于液態烴 |
| 鄰硝基甲苯 | 1.162 | 222 | 不溶于水,易溶于液態烴 |

分析 制備一硝基甲苯:分別量取10 mL和30 mL的濃硫酸和濃硝酸,將濃硝酸倒入燒杯中,濃硫酸沿著燒杯內壁緩緩注入,并不斷攪拌,配制混合溶液(即混酸)共40mL,因反應液體沸點較低,加熱時容易發生暴沸,所以在三頸瓶中加入沸石,然后加入13g甲苯(易揮發沸點為110.6℃),再向三頸瓶中加入混酸,水浴(水的沸點100℃)目的能均勻加熱,且便于控制反應速率,溫度約為50℃,反應大約10min,三頸瓶底有大量淡黃色油狀液體出現;兩種一硝基化合物都為有機物,所以只能利用它們沸點的不同采用蒸餾的方法分離,經提純最終得到純凈的一硝基甲苯,本實驗實際制得純凈的一硝基甲苯共15g.
(1)反應物甲苯沸點低,加熱時容易發生暴沸;
(2)冷凝管用于將蒸汽冷卻為液體,冷凝水應是下進上出,延長熱量交換時間,使熱量能更充分交換,確保氣體充分冷凝;
(3)儀器A是分液漏斗,使用前必須檢查是否漏液;
(4)因為分離得到的是無機和有機兩種液體,而有機物和無機物是不相溶的,因此方法是分液;分離兩種一硝基化合物只能利用它們沸點的不同,因此采用蒸餾的方法,根據蒸餾所需儀器分析解答;
(5)根椐方程式可知,一摩爾的甲苯可以得到一摩爾的對硝基甲苯與一摩爾的鄰硝基甲苯,本實驗中分離出一硝基甲苯,經提純最終得到純凈的一硝基甲苯共15g,根據方程克制13g甲苯理論產生硝基甲苯的質量,產率的計算方法就是用實際產量除以理論產量.
解答 解:(1)甲苯的沸點為110.6℃易揮發,容易發生暴沸,需用碎瓷片(沸石),
故答案為:沸石(或碎瓷片);防止暴沸;
(2)冷凝管用于將蒸汽冷卻為液體,故冷凝管的作用是冷凝回流,蒸餾時,冷卻水從冷凝管的下口通入,上口流出,可使冷凝管充滿冷水而進行充分冷卻,所以冷卻水從冷凝管的a端進入,
故答案為:冷凝回流;a;
(3)儀器A是分液漏斗,使用前必須檢查是否漏液,
故答案為:分液漏斗; 檢查是否漏液;
(4)因為分離得到的是無機和有機兩種液體,而有機物和無機物是不相溶的,因此操作1的名稱為分液;分離兩種一硝基化合物只能利用它們沸點的不同,因此采用蒸餾的方法,蒸餾燒瓶盛放兩種一硝基化合物混合物,酒精燈用于加熱蒸餾燒瓶,溫度計測量蒸汽的溫度,冷凝管用于將蒸汽冷卻為液體,鐵架臺用于固定蒸餾燒瓶,牛角管(尾接管)用于承接冷凝后的液體,錐形瓶用于盛放產品,所以操作2必需的玻璃儀器還有蒸餾燒瓶、冷凝管,
故答案為:分液;蒸餾燒瓶、冷凝管;
(5)產率的計算方法就是用實際產量除以理論產量;根椐方程式,一摩爾的甲苯可以得到一摩爾的對硝基甲苯與一摩爾的鄰硝基甲苯,換成質量即:92g的甲苯可以得到137g的對硝基苯和鄰硝基苯,則13g的甲苯就能得到的一硝基苯的質量為:$\frac{13×137}{92}$=19.35g,本實驗中分離出一硝基甲苯,經提純最終得到純凈的一硝基甲苯共15g,所以一硝基苯的產量為:$\frac{15g}{19.35g}$×100%≈77.5%,
故答案為:77.5%.
點評 本題主要考查一硝基甲苯的制備,涉及實驗流程、產率的計算等知識,明確物質的制備原理即流程的意義與目的為解答此類題的關鍵,充分考查了學生靈活應用所學知識的能力,題目難度中等.


 備戰中考寒假系列答案
備戰中考寒假系列答案科目:高中化學 來源: 題型:選擇題
| A. | 能全部透過半透膜 | B. | 所得物質一定為懸濁液或乳濁液 | ||
| C. | 所得混合物一定能導電 | D. | 有丁達爾效應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
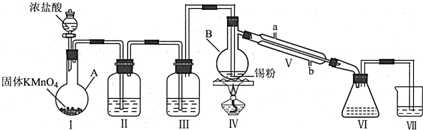
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
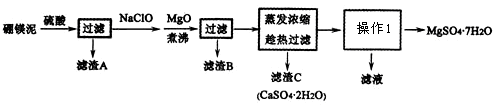
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
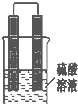 甲同學想利用原電池反應檢測金屬的活動性順序,他使用鎂片與鋁片作電極,放入 稀H2SO4溶液中,如圖所示•
甲同學想利用原電池反應檢測金屬的活動性順序,他使用鎂片與鋁片作電極,放入 稀H2SO4溶液中,如圖所示•查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 該溶液中HA有0.1%發生了電離 | |
| B. | 此酸電離平衡常數約為10-7 | |
| C. | 升高溫度后溶液的PH增大 | |
| D. | 若將PH=2的HA溶液與PH=12的NaOH溶液等體積混合后PH=7 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com