
| ||
| ||
| ||
| ||
| 88g |
| 44g/mol |
| 0.224L |
| 22.4L/mol |


 開心快樂假期作業暑假作業西安出版社系列答案
開心快樂假期作業暑假作業西安出版社系列答案 名題訓練系列答案
名題訓練系列答案科目:高中化學 來源: 題型:
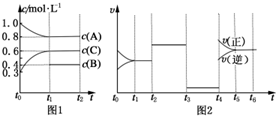 向體積為2L的密閉容器中充入2mol A、0.6mol C和一定量的B三種氣體,一定條件下發生反應2A(g)+B(g)?3C(g)△H>0,各物質的濃度隨時間變化的關系如圖1所示,其中t0~t1階段c(B)未畫出.圖2為反應體系中反應速率隨時間變化的情況,且t2,t3,t4各改變一種不同的條件.
向體積為2L的密閉容器中充入2mol A、0.6mol C和一定量的B三種氣體,一定條件下發生反應2A(g)+B(g)?3C(g)△H>0,各物質的濃度隨時間變化的關系如圖1所示,其中t0~t1階段c(B)未畫出.圖2為反應體系中反應速率隨時間變化的情況,且t2,t3,t4各改變一種不同的條件.查看答案和解析>>
科目:高中化學 來源: 題型:
 HR是含Z元素的一元酸.室溫時,用0.250mol?L-1 NaOH溶液滴定25.0mL HR溶液時,溶液的pH變化情況如圖所示.其中,a點表示兩種物質恰好完全反應.
HR是含Z元素的一元酸.室溫時,用0.250mol?L-1 NaOH溶液滴定25.0mL HR溶液時,溶液的pH變化情況如圖所示.其中,a點表示兩種物質恰好完全反應.查看答案和解析>>
科目:高中化學 來源: 題型:

查看答案和解析>>
科目:高中化學 來源: 題型:

查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:

| A、CO2(g)和CaO(s)的總能量大于CaCO3(s)的總能量 |
| B、該反應的焓變大于零 |
| C、該反應中有離子鍵斷裂也有共價鍵斷裂,化學鍵斷裂吸收能量,化學鍵生成放出能量 |
| D、由該反應可推出凡是需要加熱才發生的反應均為吸熱反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、該反應中既有舊化學鍵的斷裂,也有新化學鍵的生成 |
| B、該反應中每消耗1molNa,則同時消耗18gH2O,產生1molNaOH和11.2LH2(標況下) |
| C、由于該反應常溫下能自動進行,所以該反應一定是放熱反應 |
| D、由于該反應是放熱反應,所以斷裂舊化學鍵所吸收的能量一定比形成新化學鍵所放出的能量少 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com