
科目:高中化學 來源:2017屆北京市豐臺區高三上學期期末化學試卷(解析版) 題型:選擇題
下列有關性質的比較,不能用元素周期律解釋的是
A. 酸性:H2SO4 >HClO B. 金屬性:Na>Mg
C. 堿性:KOH>NaOH D. 熱穩定性:HC1>HBr
查看答案和解析>>
科目:高中化學 來源:2016-2017學年吉林省長春市五縣高二上期末化學試卷(解析版) 題型:選擇題
常溫下,物質的量濃度均為0.1mol·L-1的下列四種溶液,其中pH最小的是( )
A.NaCl B.Ba(OH)2 C.NH4Al(SO4)2 D.Na3PO4
查看答案和解析>>
科目:高中化學 來源:2016-2017學年黑龍江、吉林省兩省六校高一上期中化學試卷(解析版) 題型:選擇題
在酸性溶液中能大量共存,并且溶液為無色透明的是( )
A.K+、Ca2+、HCO3-、Cl- B.Cu2+、Na+、NO3-、Cl-
C.Na+、K+ 、Mg2+、SO42- D.Mg2+、Fe3+、Cl-、OH-
、Mg2+、SO42- D.Mg2+、Fe3+、Cl-、OH-
查看答案和解析>>
科目:高中化學 來源:2016-2017學年黑龍江、吉林省兩省六校高一上期中化學試卷(解析版) 題型:選擇題
下列化學反應,能用離子方程式H++OH- = H2O來表示的是( )
A.硫酸和NaOH溶液 B.醋酸和氫氧化鉀溶液
C.鹽酸和氫氧化鎂 D.稀硝酸和氨水混合
查看答案和解析>>
科目:高中化學 來源:2016-2017學年黑龍江、吉林省兩省六校高二上期中化學試卷(解析版) 題型:填空題
科學家利用太陽能分解 水生成的氫氣在催化劑作用下與二氧化碳反應生成甲醇,并開發出直接以
水生成的氫氣在催化劑作用下與二氧化碳反應生成甲醇,并開發出直接以 甲醇為燃料的燃料電池。請回答下列問題:
甲醇為燃料的燃料電池。請回答下列問題:
(1)已知:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) △H=+49.0kJ/mol
②CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g) △H=-192.9kJ/mol
由上述方程式可知,CH3OH(g)的燃燒熱__________(填“大于”、“等于”或小于”)192.9kJ/mol。已知水的汽化熱為44 kJ/mol,則表示氫氣燃燒熱的熱化學方程式為__________________________。
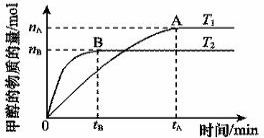
(2)在容積為2 L的密閉容器中,由CO2和H2合成甲醇,在其他條件不變的情況下,考查溫度對反應的影響,實驗結果如下圖所示(注:T1、T2均大于300 ℃)該反應為_________反應(填“放熱”或“吸熱”);在T1溫度時,將1 mol CO2和3 mol H2充入一密閉恒容容器中,充分反應達到平 衡后,若CO2轉化率為a,則容器內的壓強與起始壓強之比為____________________。
衡后,若CO2轉化率為a,則容器內的壓強與起始壓強之比為____________________。
查看答案和解析>>
科目:高中化學 來源:2016-2017學年黑龍江、吉林省兩省六校高二上期中化學試卷(解析版) 題型:選擇題
已知
①H2(g)+1/2O2(g)=H2O(l) △H =-284.2kJ /mo1
②2NH3(g)+3/2O2(g)=N2(g)+3 H2O(l) △H =-760.2 kJ /mo1
則可推知1/2 N2(g)+ 3/2H2(g)= NH3(g) 的△H是( )
A.-91.96 kJ/mol B.-104.5 kJ/mol
C.+476.52 kJ/mol D.-46.2 kJ/mol
查看答案和解析>>
科目:高中化學 來源:2017屆廣東省惠州市高三上第三次調研化學試卷(解析版) 題型:實驗題
如圖A、B、C、D、E五組儀器(圖中a、b、c表示止水夾)可以根據需要組裝成不同實驗裝置.某興趣小組的同學利用這些實驗儀器進行實驗,請對其方案進行完善或評價.
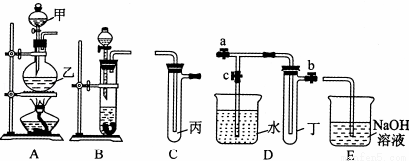
(1)將B、C、E相連,用濃硫酸和濃鹽酸可制取氯化氫,裝在分液漏斗中的試劑是 ,該實驗尾氣吸收裝置設計有何不妥? ;改正后將B、D、E裝置相連,用D裝置中的丁試管收集滿氯化氫氣體,使燒杯中的水進入試管丁的操作是 。
(2)將A、C、E相連,并在丙中加入適量水,即可制得氯水,將所得氯水分為兩份,進行ⅠⅡ兩個實驗,實驗操作、現象、結論如下表所示:
序號 | 實驗操作 | 現象 | 結論 |
Ⅰ | 將氯水滴入品紅溶液 | 品紅溶液褪色 | 氯氣與水反應的產物有漂白性 |
Ⅱ | 氯水中加入碳酸氫鈉粉末 | 有無色氣泡產生 | 氯氣與水反應的產物有具有酸性 |
請你評價:實驗I推出的相應的結論是否合理? ;若不合理,請說明理由,〔若合理則無需填寫) 。實驗Ⅱ推出的結論是否合理? ;若不合理,請說明理由,(若合理則無需填寫) 。
(3)研究表明,用ClO2氣體對自來水消毒效果比用Cl2更好.市售的一種新型消毒劑含兩種成分,分別是NaClO3和Na2C2O4.兩種成分在溶液中混合便產生ClO2,反應的化學方程式為 。
查看答案和解析>>
科目:高中化學 來源:2017屆福建省高三上聯考二化學卷(解析版) 題型:選擇題
在一定溫度下,將氣體X和氣體Y各0.16mol充入10L恒容密閉容器中,發生反應X(g) + Y(g)  2Z(g) △H<0,一段時間后達到平衡,反應過程中測定的數據如下表:
2Z(g) △H<0,一段時間后達到平衡,反應過程中測定的數據如下表:
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列說法正確的是
A.0~2min的平均速率ν(Z) = 2.0×10-3mol·L-1·min-1
B.其他條件不變,降低溫度,反應達到新平衡前ν(逆)>ν(正)
C.該溫度下此反應的平衡常數K =1.44
D.其他條件不變,再充入0.2molZ,平衡時X的體積分數增大
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com