
氫氣是一種清潔能源,又是合成氨工業的重要原料。
(1)已知:CH4(g)+H2O==CO+3H2(g) △H=206.2 kJ·mol-1。
CH4(g)+CO2(g)==2CO(g)+2H2(g) △H=247.4 kJ·mol-1
甲烷和H2O(g)反應生成H2和CO2的熱化學方程式為___________________。
(2)工業合成氨的反應原理為N2(g)+3H2(g) 2NH3(g) △H=-92.4 kJ·mol-1。
2NH3(g) △H=-92.4 kJ·mol-1。
某溫度下,把10 mol N2與28 mol H2置于容積為10 L的密閉容器內,10 min時反應達到平衡狀態,測 得氮氣的平衡轉化率為60%,則10 min內該反應的平均速率v(NH3)=__________mol·L-1·min-1,該溫度下該反應的平衡常數K=________。 欲增大氮氣的平衡轉化率,可采取的措施有_____________、____________等(共寫兩條措施即可,每空一條)。
(3)下圖所示裝置工作時均與H2有關。

圖l所示裝置中陽極的電極反應式為______________。
②圖2所示裝置中,通入H2的管口是_____________(選填字母代號)。
③某同學按圖3所示裝置進行實驗,實驗結束后.將玻璃管內固體物質冷卻后,溶于稀硫酸,充分反應后,滴加KSCN溶液。溶液不變紅,再滴入新制氯水,溶液變為紅色。該同學據此得出結論:鐵與水蒸氣反應生成FeO和H2。該結論_____________(填“嚴密”或“不嚴密”),你的理由是(用離子方程式和必要的文字說明)______________________。
科目:高中化學 來源:2017屆湖南省高三上學期9月月考化學試卷(解析版) 題型:選擇題
鋅與很稀的硝酸反應生成硝酸鋅、硝酸銨和水.當生成1mol硝酸鋅時,被還原的硝酸的物質的量為( )
A.2mol B.1 mol C.0.5mol D.0.25mol
查看答案和解析>>
科目:高中化學 來源:2017屆湖北省沙市高三上學期第二次考試化學試卷(解析版) 題型:選擇題
利用焰色反應,人們在煙花中有意識地加入特定金屬元素,使焰火更加絢麗多彩。下列說法中正確的是
A. 非金屬單質燃燒時火焰均為無色 B. NaCl與Na2CO3灼燒時火焰顏色相同
C. 焰色反應均應透過藍色鈷玻璃觀察 D. 只有金屬單質灼燒時火焰才有顏色
查看答案和解析>>
科目:高中化學 來源:2017屆湖北省高三上學期8月摸底化學試卷(解析版) 題型:選擇題
下列說法不正確的是( )
A.為除去FeCl2溶液中少量的FeCl3,可加入過量鐵粉,再過濾
B.明礬中Al3+水解產生具有吸附性的膠體,明礬可用于自來水的凈化
C.為除去CO2中少量的HCl,可使其通過飽和的Na2CO3溶液
D.為除去KCl溶液中少量的MgCl2,可加入適量KOH溶液,再過濾
查看答案和解析>>
科目:高中化學 來源:2017屆湖北省高三上學期8月摸底化學試卷(解析版) 題型:選擇題
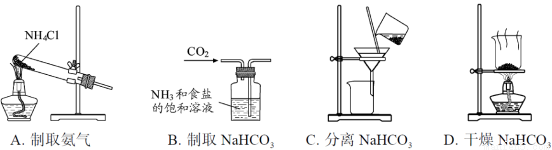
根據侯氏制堿原理制 備少量NaHCO3的實驗,經過制取氨氣、制取NaHCO3、分離NaHCO3、干燥NaHCO3四個步驟,下列圖示裝置和原理能達到實驗目的的是( )
備少量NaHCO3的實驗,經過制取氨氣、制取NaHCO3、分離NaHCO3、干燥NaHCO3四個步驟,下列圖示裝置和原理能達到實驗目的的是( )
查看答案和解析>>
科目:高中化學 來源:2017屆山東省高三第一次診斷性考試化學試卷(解析版) 題型:選擇題
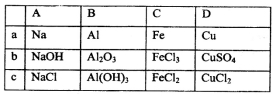
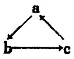
Na、Al、Fe、Cu是中學化學中重要的金屬元素。它們的單質及其化合物之間有很多轉化關系。下表所列物質不能按如圖(“→”表示一步完成)關系相互轉化的是
查看答案和解析>>
科目:高中化學 來源:2017屆山東省高三第一次診斷性考試化學試卷(解析版) 題型:選擇題
新型陶瓷A1N可通過反應: A12O3+N2+3C 2A1N+3CO合成。下列正確的是
2A1N+3CO合成。下列正確的是
A.上述反應中,N2是還原劑,A12O3是氧化劑
B.A1N中氮元素的化合價為+3
C.上述反應中,每生成1 mol A1N需轉移3 mol電子
D.A1N的摩爾質量為41 g
查看答案和解析>>
科目:高中化學 來源:2017屆江西省高三上第一次月考化學試卷(解析版) 題型:選擇題
假設與猜想是科學探究的先導和價值所在。 下列假設引導下的探究肯定沒有意義的是
A.探究Na與水的反應可能有O2生成
B.探究SO2和Na2O2反應可能有Na2SO4生成
C.探究足量的銅與一定量的濃硝酸反應的氣體產物是NO還是NO2
D.探究向滴有酚酞試液的NaOH溶液中通入一定量Cl2后,酚酞試液紅色褪去的現象是溶液的酸堿性改變所致,還是HClO的漂白性所致
查看答案和解析>>
科目:高中化學 來源:2017屆內蒙古高三上第一次月考化學試卷(解析版) 題型:填空題
Ⅰ:現有下列7種物質:①NaHCO3②CH3COOH③BaSO4;④HF;⑤C2H5OH;⑥Al;⑦食鹽水.其中屬于強電解質的是 (填序號,下同),既能跟鹽酸反應又能跟NaOH溶液反應的是 .
II:現有一瓶濃度為0.2mol/L的某酸溶液,可能為醋酸、鹽酸、硫酸中的一種,為了確定該酸溶液的組成進行實驗:取20.00mL該酸溶液,逐滴加入0.2mol/L的氫氧化鈉溶液,恰好反應完全時所需堿液體積為20.00mL,請用化學用語回答:
(1)該酸不可能是 ;
(2)用pH試紙測得反應后所得溶液呈堿性,根據此現象說明該酸溶液為 ,用離子方程式說明溶液呈堿性的原因 ;
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com