
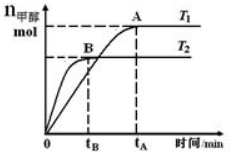
 在恒容密閉容器中,由CO合成甲醇:CO(g)+2H2(g)?CH3OH(g),在其他條件不變的情況下,研究溫度對反應的影響,實驗結果如圖所示.下列說法正確的是( )
在恒容密閉容器中,由CO合成甲醇:CO(g)+2H2(g)?CH3OH(g),在其他條件不變的情況下,研究溫度對反應的影響,實驗結果如圖所示.下列說法正確的是( )| A. | CO合成甲醇的反應為吸熱反應 | |
| B. | 該反應在T1時的平衡常數比T2時的大 | |
| C. | 平衡常數K=$\frac{c(CO)•{c}^{2}({H}_{2})}{c(C{H}_{2}OH)}$ | |
| D. | 處于A點的反應體系從T1變到T2,達到平衡時$\frac{n({H}_{2})}{n(C{H}_{3}OH)}$減小 |
分析 A.由圖可知,T2溫度下到達平衡所以時間較短,反應速率較快,故溫度T2>T1.溫度越高,平衡時甲醇的物質的量越小,說明升高溫度平衡向逆反應方向移動,據此判斷;
B.由圖可知,T2溫度下到達平衡所以時間較短,反應速率較快,故溫度T2>T1,溫度越高,平衡時甲醇的物質的量越小,說明升高溫度平衡向逆反應方向移動,據此判斷;
C.化學平衡常數,是指在一定溫度下,可逆反應達到平衡時各生成物濃度的化學計量數次冪的乘積除以各反應物濃度的化學計量數次冪的乘積所得的比值,據此書寫;
D.由圖可知,處于A點的反應體系從T1變到T2,溫度增大,平衡向逆反應方向移動,據此分析.
解答 解:A.由圖可知,T2溫度下到達平衡所以時間較短,反應速率較快,故溫度T2>T1.溫度越高,平衡時甲醇的物質的量越小,說明升高溫度平衡向逆反應方向移動,所以合成甲醇的反應為放熱反應,故A錯誤;
B.由圖可知,T2溫度下到達平衡所以時間較短,反應速率較快,故溫度T2>T1.溫度越高,平衡時甲醇的物質的量越小,說明升高溫度平衡向逆反應方向移動,化學平衡常數降低,在T1時的平衡常數比T2時的大,故B正確;
C.CO(g)+2H2(g)?CH3OH(g)的平衡常數表達式k=$\frac{c(C{H}_{3}OH)}{c(CO){•c}^{2}({H}_{2})}$,故C錯誤;
D.由圖可知,處于A點的反應體系從T1變到T2,溫度增大,平衡向逆反應方向移動,氫氣物質的量增大,甲醇的物質的量減小,$\frac{n({H}_{2})}{n(C{H}_{3}OH)}$增大,故D錯誤;
故選B.
點評 本題考查化學平衡圖象、化學平衡影響因素、化學平衡常數等,難度中等,注意理解外界條件對化學平衡的影響.


科目:高中化學 來源: 題型:選擇題
| A. | Cl2是氧化劑 | B. | I2是還原產物 | ||
| C. | 上述反應屬于置換反應 | D. | 上述反應屬于離子反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | H2、I2、HI平衡混合氣體加壓顏色變深 | |
| B. | 氯水光照顏色變淺 | |
| C. | NO2、N2O4混合氣體加熱顏色變深 | |
| D. | FeCl和KSCN的混合溶液中加入FeCl3固體,溶液顏色加深 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
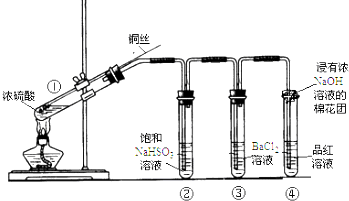
| 加入試劑 | 現象 | 反應的離子方程式 | |
| 第一份 | 加入NaOH溶液 | 有白色沉淀生成 | SO2+2OH-═SO32-+H2OBa2++SO32-═BaSO3↓ |
| 第二份 | 加入氯水 | 有白色沉淀生成 | SO2+Cl2+H2O═4H++2Cl-+SO42-Ba2++SO42-═BaSO4↓ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 過濾 | B. | 蒸發(fā) | C. | 萃取 | D. | 結晶 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | $\frac{n(S{O}_{2})}{n({H}_{2})}$=$\frac{1}{1}$ | B. | $\frac{n(S{O}_{2})}{n({H}_{2})}$=$\frac{4}{1}$ | C. | $\frac{n(S{O}_{2})}{n({H}_{2})}$=$\frac{1}{4}$ | D. | $\frac{n(S{O}_{2})}{n({H}_{2})}$=$\frac{3}{2}$ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NH3、O2、HCl | B. | N2、O2、CO2 | C. | CO2、NO、O2 | D. | N2、H2S Cl2 |
查看答案和解析>>
湖北省互聯(lián)網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com