
分析 (1)Na、K能和水反應生成氫氣,在氧氣中燃燒生成過氧化物,過氧化鈉和水、二氧化碳反應都生成氧氣,促進鈉、鉀燃燒;
(2)氯化銨屬于離子化合物,含有離子鍵和共價鍵;
(3)NaCN屬于離子化合物,C、N原子周圍都是8個電子;Na+原子核外有10個電子;根據(jù)C的電子排布判斷;N的原子核有7個電子,最外層有5個;比較兩種元素的非金屬性強弱,可根據(jù)單質(zhì)之間的置換反應、與氫氣反應的難易程度、氫化物的穩(wěn)定性以及最高正價氧化物對應水化物酸性強弱;
(4)根據(jù)元素守恒確定X中元素,根據(jù)轉(zhuǎn)移電子守恒、原子守恒確定X化學式;
(5)根據(jù)題意可知,酸性條件下CNO-與NaClO反應生成N2、CO2和Cl2,根據(jù)氧化還原反應配平.
解答 解:(1)Na、K能和水反應生成氫氣,在氧氣中燃燒生成過氧化物,過氧化鈉和水、二氧化碳反應都生成氧氣,促進鈉、鉀燃燒,所以應該采用細沙滅火,
故答案為:D;
(2)氯化銨屬于離子化合物,含有離子鍵和共價鍵,氯化銨分解時破壞了共價鍵和離子鍵;
故答案為:離子鍵、共價鍵;
(3)NaCN屬于離子化合物,C、N原子周圍都是8個電子,其電子式為:Na+[:C┇┇N:]-;Na+原子核外有10個電子,每個電子一種運動狀態(tài),共10種運動狀態(tài)不同的電子;C的電子排布式為1s22s22p2,共有3種能量不同的電子;N的原子核有7個電子,最外層有5個,根據(jù)其電子式可知,含有1個孤電子對;
A.相同條件下水溶液的pH:NaHCO3>NaNO3,說明硝酸的酸性強于碳酸,則證明非金屬性N>C,故A正確;
B.酸性:HNO2>H2CO3,由于亞硝酸不是N元素的最高價氧化物對應的水化物,無法比較二者的非金屬性大小,故B錯誤;
C、CH4的穩(wěn)定性比NH3弱,與實際不符,故C錯誤;
D、C 與H2的化合比N2與H2的化合更困難,與實際不符,故D錯誤;
故答案為:Na+[:C┇┇N:]-;10;3;1;A;
(4)根據(jù)元素守恒知,X中含有Na、C元素,該反應中N元素化合價由-3價轉(zhuǎn)化為0價、NaCN中C元素化合價為+2價,則C元素化合價由+2價轉(zhuǎn)化為+4價,轉(zhuǎn)移電子數(shù)為6,根據(jù)轉(zhuǎn)移電子守恒、原子守恒知X為NaHCO3,
故答案為:NaHCO3;
(5)根據(jù)題意可知,酸性條件下CNO-與NaClO反應生成N2、CO2和Cl2,反應離子方程式為2CNO-+6ClO-+8H+═N2↑+2CO2↑+3Cl2↑+4H2O;
故答案為:2CNO-+6ClO-+8H+═N2↑+2CO2↑+3Cl2↑+4H2O..
點評 本題考查了元素化合物的性質(zhì)、電子式、化學鍵、非金屬性強弱比較、氧化還原反應等,側(cè)重于考查學生的對基礎知識的應用能力,注意把握元素化合物的性質(zhì)以及反應中元素的化合價變化為解答的關鍵,題目難度中等.


科目:高中化學 來源: 題型:選擇題
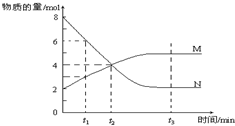
| A. | 該反應的化學方程式為:2 M?N | |
| B. | t1時,V正>V逆 | |
| C. | t2時,V正=V逆,達到平衡 | |
| D. | t 3時,M、N的濃度不再發(fā)生變化,反應停止 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 原子半徑:Z>Y>X | |
| B. | 最高價氧化物的水化物的酸性:Y>Z | |
| C. | 化合物WZ2中各原子均滿足8電子的穩(wěn)定結(jié)構(gòu) | |
| D. | Y、Z均能與碳元素形成共價化合物 |
查看答案和解析>>
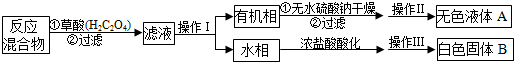
科目:高中化學 來源: 題型:解答題
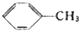 $→_{△}^{KMnO_{4}}$
$→_{△}^{KMnO_{4}}$ $\stackrel{HCl}{→}$
$\stackrel{HCl}{→}$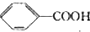
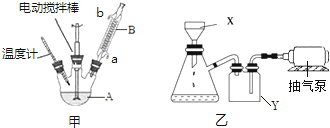
| 名稱 | 相對分子質(zhì)量 | 性狀 | 熔點(℃) | 沸點(℃) | 溶解性 | |
| 水 | 乙醇 | |||||
| 甲苯 | 92 | 無色液體、易燃、易揮發(fā) | -95 | 110.6 | 不溶 | 互溶 |
| 苯甲酸 | 122 | 白色片狀或針狀晶體 | 112.4(100℃升華) | 248 | 微溶 | 易溶 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A | B | C | D |
 |  |  | 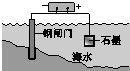 |
| 鋼鐵表面水膜的酸性很弱或呈中性,發(fā)生吸氧腐蝕 | 鋼鐵表面水膜的酸 性較強,發(fā)生析氫 腐蝕 | 將鋅板換成銅板對 鋼閘門保護效果更好 | 鋼閘門作為陰極而受到保護 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 砷元素的最高化合價為+3 | B. | 砷元素是第四周期的主族元素 | ||
| C. | 砷原子的次外層上有8個電子 | D. | 砷的氧化物的水化物是強酸 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 與H2化合時,X單質(zhì)比Y單質(zhì)容易 | |
| B. | X的最高價氧化物的水化物的酸性比Y的最高價氧化物的水化物的酸性強 | |
| C. | X原子的原子序數(shù)比Y原子的原子序數(shù)大 | |
| D. | X單質(zhì)可以把Y從其氫化物中置換出來 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | FeCl2>HI>H2SO3 | B. | HI>FeCl2>H2SO3 | C. | H2SO3>HI>FeCl2 | D. | FeCl2>H2SO3>HI |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
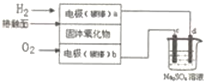
| A. | 電路中電子流向為a→d→c→b | |
| B. | 電極b為負極,電極反應式為O2+4e一=2O2- | |
| C. | 電解后燒杯中溶液pH增大 | |
| D. | 理論上b極消耗氣體和c極生成氣體質(zhì)量相等 |
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com