
| 物質 | CH4 | CO2 | CO | H2 |
| 體積分數 | 0.1 | 0.1 | 0.4 | 0.4 |

分析 (1)①設反應了CO2x,列三段式,根據體積分數計算x,代入化學平衡常數計算;
②已知:ⅠCH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3kJ•mol-1
ⅡCO(g)+H2O (g)═CO2(g)+H2 (g)△H=+2.8kJ•mol-1
Ⅲ2CO(g)+O2(g)═2CO2(g)△H=-566.0kJ•mol-1
由蓋斯定律Ⅰ+Ⅱ×2-Ⅲ×2可得CO2(g)+CH4(g)?2CO(g)+2H2(g),據此計算;
(2)①根據溫度對催化劑活性的影響;
②根據外界條件對化學平衡的影響,平衡正向移動,反應物轉化率增大;
③先將Cu2Al2O4拆成氧化物的形式:Cu2O•Al2O3,再根據氧化物與酸反應生成離子方程式,需要注意的是一價銅具有還原性;
(3)①二氧化碳為酸性氣體,Li2O、Na2O、MgO均能吸收CO2與氧化性無關;
②根據題干信息,反應物為CO2與Li4SiO4,生成物有Li2CO3,根據質量守恒進行解答;
(4)二氧化碳、水分別在a極得到電子發生還原反應生成一氧化碳、氫氣,同時生成氧離子.
解答 解:(1)①250℃時,以鎳合金為催化劑,向4L容器中通入6mol CO2、6mol CH4,反應了CO2x:
CO2(g)+CH4(g)?2CO(g)+2H2(g)
n始:6 6 0 0
n轉:x x 2x 2x
n平:6-x 6-x 2x 2x
由CO2的體積分數為0.1,則$\frac{6-x}{6-x+6-x+2x+2x}$=0.1,解得x=4,則K=$\frac{(8mol÷4L)^{4}}{(2mol÷4L)^{2}}$=64;
故答案為:64;
②已知:ⅠCH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3kJ•mol-1
ⅡCO(g)+H2O (g)═CO2(g)+H2 (g)△H=+2.8kJ•mol-1
Ⅲ2CO(g)+O2(g)═2CO2(g)△H=-566.0kJ•mol-1
由蓋斯定律Ⅰ+Ⅱ×2-Ⅲ×2可得CO2(g)+CH4(g)?2CO(g)+2H2(g)△H=-890.3kJ•mol-1+2.8kJ•mol-1×2+566.0kJ•mol-1×2=+247.3 kJ•mol-1;
故答案為:+247.3 kJ•mol-1;
(2)①溫度超過250℃時,催化劑的催化效率降低,所以溫度升高而乙酸的生成速率降低;
故答案:溫度超過250℃時,催化劑的催化效率降低;
②增大反應壓強、增大CO2的濃度,平衡正向移動,反應物轉化率增大;
故答案為:增大反應壓強、增大CO2的濃度;
③Cu2Al2O4拆成氧化物的形式:Cu2O•Al2O3,與酸反應生成離子方程式:3Cu2Al2O4+32H++2NO3-=6Cu2++6Al3++2NO↑+16H2O;
故答案為:3Cu2Al2O4+32H++2NO3-=6Cu2++6Al3++2NO↑+16H2O;
(3)①a.Li2O、Na2O、MgO均屬于堿性氧化物,均能吸收酸性氧化物CO2,可在堿性氧化物中尋找吸收CO2的其他物質,故a正確;
b.Li2O、Na2O、MgO均能吸收CO2,鈉、鎂、鋁為ⅠA、ⅡA族元素,所以可在ⅠA、ⅡA族元素形成的氧化物中尋找吸收CO2的其他物質,故b正確;
c.Li2O、Na2O、MgO均能吸收CO2,但它們都沒有強氧化性,且吸收二氧化碳與氧化還原無關,故c錯誤;
故答案為:ab;
②在500℃,CO2與Li4SiO4接觸后生成Li2CO3,反應物為CO2與Li4SiO4,生成物有Li2CO3,根據質量守恒可知產物還有Li2SiO3,所以化學方程式為:CO2+Li4SiO4$?_{700℃}^{500℃}$ Li2CO3+Li2SiO3;
故答案為:CO2+Li4SiO4$?_{700℃}^{500℃}$ Li2CO3+Li2SiO3;
(4)二氧化碳在a極得到電子發生還原反應生成一氧化碳同時生成氧離子,反應電極反應式為:CO2+2e-═CO+O2-;
故答案為:CO2+2e-═CO+O2-.
點評 本題考查了綜合利用CO2,涉及蓋斯定律以及化學反應常數、化學平衡以及原電池原理的運用,難度中等,掌握基礎,分析題目信息,根據所學知識即可完成.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:選擇題
| A. | 離子半徑:F->Mg2+>Al3+ | B. | 熱穩定性:HCl>H2S>AsH3 | ||
| C. | 酸性:H3AlO3<H2CO3<H3PO4 | D. | 水溶性:SO2<H2S<NH3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Fe、MnO2 | B. | C、FeS | C. | Si、FeO | D. | CuO、Ag2S |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
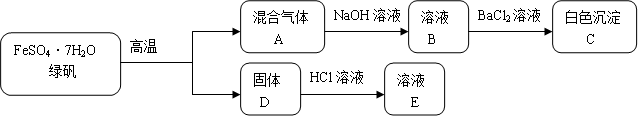
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
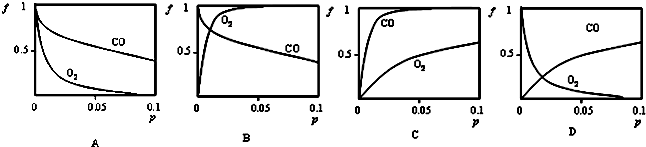

查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
 在容積為1.00L的容器中,通入一定量的N2O4,發生反應N2O4(g)?2NO2(g),隨溫度升高,混合氣體的顏色變深.回答下列問題:
在容積為1.00L的容器中,通入一定量的N2O4,發生反應N2O4(g)?2NO2(g),隨溫度升高,混合氣體的顏色變深.回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
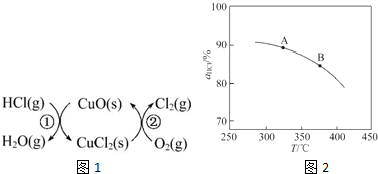
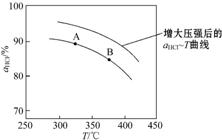 ,并簡要說明理由:增大壓強,平衡向正反應方向移動,αHCl增大,相同溫度下HCl的平衡轉化率比之前實驗的大.
,并簡要說明理由:增大壓強,平衡向正反應方向移動,αHCl增大,相同溫度下HCl的平衡轉化率比之前實驗的大.| t/min | 0 | 2.0 | 4.0 | 6.0 | 8.0 |
| n(Cl2)/10-3mol | 0 | 1.8 | 3.7 | 5.4 | 7.2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2SO2(g)+O2(g)?2SO3(g);△H=-2a KJ/mol | B. | 2SO2(g)+O2(g)2?SO3(g);△H=-a KJ/mol | ||
| C. | SO2(g)+$\frac{1}{2}$O2(g)?SO3(g);△H=a KJ/mol | D. | SO2(g)+$\frac{1}{2}$O2(g)?SO3(g);△H=-2a KJ/mol |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 銅全部溶解,且溶液為藍色,有紅棕色氣體產生 | |
| B. | 銅部分溶解,且溶液為藍色,有紅棕色氣體產生 | |
| C. | 銅全部溶解,且溶液為藍色,有無色氣體產生 | |
| D. | 銅部分溶解,且溶液為藍色,有無色氣體產生 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com