
分析 A、B、C、D、E、F、G元素原子序數依次增大.C原子最外層電子數與核外電子總數之比為3:4,最外層電子數不能超過8,原子只能有2個電子層,最外層電子數為6,故C為O元素;E與C同主族,則E為S元素;B原子最外層有3個未成對電子,原子核外電子排布為1s22s22p3,故B為N元素;F-、D+、A+離子的半徑逐漸減小,化合物AF常溫下為氣體,則A為H元素、D為Na、F為Cl,G的基態原子核外M能層填滿電子,N能層只有1個電子,則G為Cu元素,據此解答.
(1)D為Na,原子核外有11個電子,根據能量最低原理書寫核外電子排布;N元素2p能級為半滿穩定狀態,能量較低,第一電離能高于氧元素的,同主族張而行第一電離能減小;
(2)A與C可形成18電子分子為H2O2,其水溶液中滴入少量氯化鐵溶液時,分解生成水與氧氣;
(3)由上述七種元素中的三種元素組成化合物,為常見家用消毒劑的主要成分,該化合物為NClO,溶液中次氯酸根離子水解,溶液呈堿性;
(4)G的低價氧化物是Cu2O,B的最高價氧化物的水化物是HNO3,該反應方程式為:3Cu2O+14HNO3=6Cu(NO3)2+2NO+7H2O;
(5)1mol氣態N2H4在適量O2中燃燒,生成N2和氣態H2O,放出534kJ的熱量,可得:
N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-534kJ/mol ①,
由1 mol液態H2O完全氣化需吸收44 kJ熱量,可得:
H2O(l)=H2O(g)△H=+44kJ/mol②,
根據蓋斯定律,①-②×2得N2H4(g)+O2(g)=N2(g)+2H2O(l).
解答 解:A、B、C、D、E、F、G元素原子序數依次增大.C原子最外層電子數與核外電子總數之比為3:4,最外層電子數不能超過8,原子只能有2個電子層,最外層電子數為6,故C為O元素;E與C同主族,則E為S元素;B原子最外層有3個未成對電子,原子核外電子排布為1s22s22p3,故B為N元素;F-、D+、A+離子的半徑逐漸減小,化合物AF常溫下為氣體,則A為H元素、D為Na、F為Cl,G的基態原子核外M能層填滿電子,N能層只有1個電子,則G為Cu元素.
(1)D是Na元素,鈉原子核外有11個電子,根據構造原理知D元素基態原子的核外電子排布式1s22s22p63s1;
B是N元素,C是O元素,E是S元素,N元素2p能級為半滿穩定狀態,能量較低,第一電離能高于氧元素的,同主族張而行第一電離能減小,所以B、C、E三種元素的第一電離能由大到小的順序是N>O>S,
故答案為:1s22s22p63s1;N>O>S;
(2)A是H元素,C是O元素,A與C可形成18電子分子,則該物質是H2O2,雙氧水在氯化鐵作催化劑條件下分解生成水和氧氣,反應方程式為:2H2O2$\frac{\underline{\;FeCl_{3}\;}}{\;}$2H2O+O2↑,
故答案為:2H2O2$\frac{\underline{\;FeCl_{3}\;}}{\;}$2H2O+O2↑;
(3)由三種元素組成的常見家用消毒劑的主要成分是NaClO,次氯酸鈉中鈉離子和次氯酸根離子之間存在離子鍵,氧原子和氯原子之間存在共價鍵,次氯酸鈉是強堿弱酸鹽,次氯酸根離子易水解ClO-+H2O?HClO+OH-,使其溶液呈堿性,
故答案為:離子鍵、共價鍵;ClO-+H2O?HClO+OH-;
(4)G的低價氧化物是Cu2O,B的最高價氧化物的水化物是HNO3,該反應方程式為:3Cu2O+14HNO3=6Cu(NO3)2+2NO+7H2O,根據方程式知,0.3molCu2O和1.4mol硝酸恰好完全反應,
故答案為:1.4;
(5)1mol氣態N2H4在適量O2中燃燒,生成N2和氣態H2O,放出534kJ的熱量,可得:
N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-534kJ/mol ①,
由1 mol液態H2O完全氣化需吸收44 kJ熱量,可得:
H2O(l)=H2O(g)△H=+44kJ/mol②,
根據蓋斯定律,①-②×2得N2H4(g)+O2(g)=N2(g)+2H2O(l)△H=-534kJ/mol-2(+44kJ/mol)=-622kJ/mol,
故答案為:N2H4(g)+O2(g)=N2(g)+2H2O(l)△H=-622kJ/mol.
點評 本題考查比較綜合,涉及結構性質位置關系應用、核外電子排布、電離能、蓋斯定律、鹽類水解、氧化還原反應等知識點,正確推斷元素是解本題關鍵,注意同周期第一電離能異常情況,難度中等.


 智慧小復習系列答案
智慧小復習系列答案科目:高中化學 來源: 題型:選擇題
| A. | ①②③④ | B. | ③④⑤⑥ | C. | ①③④ | D. | ①③④⑤ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①②反應均是氧化還原反應 | |
| B. | KI在整個反應過程中起催化作用 | |
| C. | KI在整個反應過程中起氧化作用 | |
| D. | “溶液突然變為藍色,隨之又很快消失”這一現象與①②的反應速率有關 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

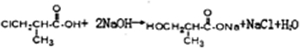 ;高分子化合物H的結構簡式為
;高分子化合物H的結構簡式為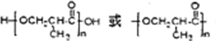 .
.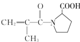 ,F有多種同分異構體,如
,F有多種同分異構體,如 等.寫出滿足下列條件的F的同分異構體的結構簡式:
等.寫出滿足下列條件的F的同分異構體的結構簡式: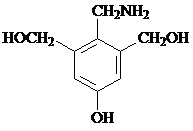 、
、 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 正反應速率 | 逆反應速率 | |
| A | vA=2 mol/(L•min) | vB=2 mol/(L•min) |
| B | vA=2 mol/(L•min) | vC=2 mol/(L•min) |
| C | vA=1 mol/(L•min) | vB=2 mol/(L•min) |
| D | vA=1 mol/(L•min) | vC=1.5 mol/(L•min) |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.3 mol•L-1的Na2SO4溶液中含有的Na+和SO42-的總物質的量為0.9 mol | |
| B. | 當1 L水吸收22.4 L氨氣時所得氨水的濃度不是1 mol•L-1,只有當22.4 L氨氣溶于水制得1 L氨水時,其濃度才是1 mol•L-1 | |
| C. | 在K2SO4和NaCl的中性混合水溶液中,如果Na+和SO42-的物質的量相等,則K+和Cl-的物質的量濃度一定相同 | |
| D. | 10℃時,0.35 mol•L-1的KCl飽和溶液100 mL蒸發掉5 g水,冷卻到10℃時,其體積小于100 mL,它的物質的量濃度仍為0.35 mol•L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com