
| 元素 | 結構、性質等信息 |
| X | 構成有機物的核心元素,該元素的一種氧化物和氣態氫化物都是典型的溫室氣體 |
| Y | 短周期中(除稀有氣體外)原子半徑最大的元素,該單質液態時可用作核反應堆的傳熱介質 |
| Z | 與Y同周期,其最高價氧化物的水化物呈兩性 |
| M | 海水中除氫、氧元素外含量最多的元素,其單質或化合物也是自來水生產過程中常用的消毒殺菌劑 |
分析 短周期元素中,X元素是構成有機物的核心元素,該元素的一種氧化物和氣態氫化物都是典型的溫室氣體,故X為C元素;Y是短周期中(除稀有氣體外)原子半徑最大的元素,該單質液態時可用作核反應堆的傳熱介質,故Y為Na;Z與Y同周期,其最高價氧化物的水化物呈兩性,故Z為Al;M是海水中除氫、氧元素外含量最多的元素,其單質或化合物也是自來水生產過程中常用的消毒殺菌劑,則M為Cl.
(1)主族元素周期數=電子層數、主族族序數=最外層電子數,碳元素相對分子質量最小的氣態氫化物為甲烷;
(2)Na+、Al3+離子電子層結構相同,核電荷數越大離子半徑越小;Y元素的最高價氧化物的水化物為NaOH,Z元素的最高價氧化物為Al2O3,二者反應生成偏鋁酸鈉與水;
(3)非金屬性越強,氫化物越穩定,可以利用最高價含氧酸的酸性強弱進行比較.
解答 解:短周期元素中,X元素是構成有機物的核心元素,該元素的一種氧化物和氣態氫化物都是典型的溫室氣體,故X為C元素;Y是短周期中(除稀有氣體外)原子半徑最大的元素,該單質液態時可用作核反應堆的傳熱介質,故Y為Na;Z與Y同周期,其最高價氧化物的水化物呈兩性,故Z為Al;M是海水中除氫、氧元素外含量最多的元素,其單質或化合物也是自來水生產過程中常用的消毒殺菌劑,則M為Cl.
(1)X為碳元素,處于周期表中第二周期第IVA族,其相對分子質量最小的氣態氫化物的化學式是CH4,
故答案為:第二周期第IVA族;CH4;
(2)Na+、Al3+離子電子層結構相同,核電荷數越大離子半徑越小,故離子半徑:Na+>Al3+,Y元素的最高價氧化物的水化物為NaOH,Z元素的最高價氧化物為Al2O3,反應離子方程式為:Al2O3+2OH-=2AlO2-+H2O,
故答案為:大;Al2O3+2OH-=2AlO2-+H2O;
(3)由于非金屬性C<Cl,故氫化物穩定性CH4<HCl,用化學方程式表示M與X兩元素的非金屬性強弱:
Na2CO3+2HClO4=2NaClO4+CO2↑+H2O,
故答案為:HCl;Na2CO3+2HClO4=2NaClO4+CO2↑+H2O.
點評 本題考查結構性質位置關系應用,比較基礎,注意掌握金屬性、非金屬性強弱比較實驗事實.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1 | B. | 3 | C. | 5 | D. | 7 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
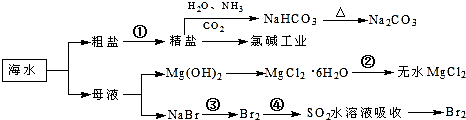
| A. | 過程①中除去粗鹽中的SO、Ca2+、Mg2+、Fe3+等雜質,加入的藥品順序為:Na2CO3溶液→NaOH溶液→BaCl2溶液→過濾后加鹽酸 | |
| B. | 步驟④的作用是達到富集溴的目的 | |
| C. | 過程②中MgCl2•6H2O加熱脫水制得無水MgCl2 | |
| D. | 工業上電解熔融精鹽的過程稱為氯堿工業 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 5.6g鐵粉在0.1mol氯氣中充分燃燒,轉移電子數為0.3NA | |
| B. | 12.5mL 16mol.L-1濃硫酸與足量銅反應,轉移電子數為0.2NA | |
| C. | 7.8g Na 2S和Na2O2 的混合物中含有的陰離子數等于0.1NA | |
| D. | 0.5mol氧單質含有NA個O2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 推廣使用太陽能、風能、海洋能、氫能,有利于緩解溫室效應 | |
| B. | 乙醇和汽油都是可再生能源,應大力推廣“乙醇汽油” | |
| C. | 用電解水的方法制取大量氫氣可以緩解能源不足的問題 | |
| D. | 電解是把化學能轉變成電能的過程 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com