

| 實驗組 | 溫度/℃ | 起始量/mol | 平衡量/mol | 達到平衡所 需時間/min | ||
| H2O | CO | H2 | CO | |||
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
分析 (1)①△G=△H-T△S<0時,反應自發進行;
②反應達到平衡狀態時,同種物質的正、逆反應速率相等,平衡時各組分的物質的量、濃度、含量等不再發生變化,以及由此衍生的其它量不變,選擇判斷的物理量,隨著反應的進行發生變化,當該物理量由變化到定值時,說明可逆反應到達平衡狀態;
(2)①根據v=$\frac{△c}{△t}$計算v(CO),再利用速率之比等于化學計量數之比計算v(CO2);
②第2組可以等效為:開始在650℃時加入1molH2O、2molCO到達平衡,保持溫度不變,再加入1molCO達到平衡,最后再升高溫度到900℃時到達平衡;開始在650℃時加入1molH2O、2molCO到達平衡,與第1組為等效平衡,轉化率相同,平衡時H2為0.8mol,保持溫度不變,再加入1molCO達到平衡,平衡正向移動,平衡時H2物質的量大于0.8mol,升高溫度到900℃時到達平衡,氫氣的物質的量減小,說明升高溫度平衡向逆反應方向移動;
(3)根據圖象知,該反應的正反應是放熱反應,能使c(CH3OH)增大,說明平衡向正反應方向移動.
解答 解:(1)①該反應△H>0,△S>0,△G=△H-T△S<0時,反應自發進行,故高溫下反應可以自發進行,故答案為:溫度;
②a.在一個容積可變的密閉容器中,容器中壓強始終不變,所以壓強不變不能說明反應到達平衡,故a錯誤;
b.l molH-H鍵斷裂的同時斷裂2mol H-O鍵,斷裂2mol H-O鍵同時生成l molH-H鍵,說明反應到達平衡,故b正確;
c.根據反應可知,自始至終v正(CO)=v正(H2O),若v正(CO)=v逆(H2O),則v正(H2O)=v逆(H2O),說明反應到達平衡,故c正確;
d.根據反應可知,自始至終c(CO)=c(H2),不能說明反應到達平衡,故d錯誤;
故選:bc;
(2)①v(CO)=$\frac{\frac{4mol-2.4mol}{2L}}{5min}$=0.16mol•(L•min)-1,速率之比等于化學計量數之,則v(CO2)=0.16mol•(L•min)-1,
故答案為:0.16mol•(L•min)-1;
②第2組可以等效為:開始在650℃時加入1molH2O、2molCO到達平衡,保持溫度不變,再加入1molCO達到平衡,最后再升高溫度到900℃時到達平衡;開始在650℃時加入1molH2O、2molCO到達平衡,與第1組為等效平衡,轉化率相同,平衡時H2為0.8mol,保持溫度不變,再加入1molCO達到平衡,平衡正向移動,平衡時H2物質的量大于0.8mol,升高溫度到900℃時到達平衡,氫氣的物質的量減小,說明升高溫度平衡向逆反應方向移動,故逆反應為吸熱反應,
故答案為:吸熱;
(3)a.升高溫度,平衡逆向移動,c(CH3OH)減小,故a錯誤;
b.充入He(g),使體系壓強增大,由于容器為恒容容器,各組分濃度不變,平衡不移動,c(CH3OH)不變,故b錯誤;
c.將H2O(g)從體系中分離出來,平衡正向移動,c(CH3OH)增大,故c正確;
d.再充入1mol CO2和3molH2,平衡正向移動,c(CH3OH)增大,故d正確.
故答案為:cd.
點評 本題考查化學平衡有關計算、平衡狀態判斷、反應自發性等,注意掌握化學平衡常數的應用,難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | 保存氫氧化鈉溶液、硅酸鈉溶液等堿性試劑,常用帶橡膠塞的玻璃瓶 | |
| B. | 保存濃硝酸及硝酸銀溶液,常用帶玻璃塞的棕色試劑瓶 | |
| C. | 保存金屬鈉和液溴時,常在試劑瓶中加入煤油進行封存 | |
| D. | 保存氫氟酸時,常用塑料瓶而不用玻璃瓶 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
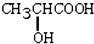 .問:
.問: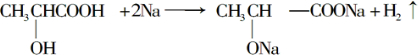
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 一定產生BaSO4沉淀 | B. | 一定產生BaSO3沉淀 | ||
| C. | 一定沒有SO2逸出 | D. | 一定有SO3逸出 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | a、b不可能是同種材料的電極 | |
| B. | 該裝置可能是電解池,電解質溶液為稀H2SO4 | |
| C. | 該裝置可能是原電池,電解質溶液為稀HNO3 | |
| D. | 反應一段時間后,斷開電路,向溶液中通入H2可使溶液復原 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 乙醇和乙酸都是常用調味品的主要成分 | |
| B. | 乙醇和乙酸的沸點和熔點都比C2H6、C2H4的沸點和熔點高 | |
| C. | 乙醇和乙酸都能發生氧化反應 | |
| D. | 乙醇和乙酸之間能發生酯化反應,酯化反應是不可逆反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
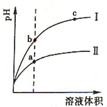 某溫度下,相同體積、相同pH的鹽酸和醋酸溶液分別加水稀釋,溶液的pH隨溶液體積變化的曲線如圖所示.下列判斷正確的是( )
某溫度下,相同體積、相同pH的鹽酸和醋酸溶液分別加水稀釋,溶液的pH隨溶液體積變化的曲線如圖所示.下列判斷正確的是( )| A. | Ⅱ為鹽酸稀釋時的pH變化曲線 | |
| B. | a點Kw的數值比c點Kw的數值大 | |
| C. | b點酸的總濃度大于a點酸的總濃度 | |
| D. | b點溶液的導電性比c點溶液的導電性強 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Cl2通入NaOH溶液中 Cl2+2OH-═Cl-+ClO-+H2O | |
| B. | 硫化亞鐵與稀硫酸反應 FeS+2H+═Fe2++H2S↑ | |
| C. | 硫酸銨和氫氧化鋇溶液 Ba2++SO42-═BaSO4↓ | |
| D. | 氫氧化鋇與稀硫酸反應 Ba2++SO42-+2H++2OH-═BaSO4↓+2H2O |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com