
| A. | 硝酸銀溶液跟銅反應 Cu+Ag+═Cu2++Ag | |
| B. | 鐵粉跟稀鹽酸反應 2Fe+6H+═2Fe3++3H2↑ | |
| C. | 硫酸和氫氧化鋇反應:H++SO42-+Ba2++OH-═H2O+BaSO4 | |
| D. | 用小蘇打治療胃酸過多:HCO3-+H+═CO2↑+H2O |
分析 A.電子、電荷不守恒;
B.反應生成氯化亞鐵和氫氣;
C.不符合離子的配比;
D.反應生成氯化鈉、水、二氧化碳.
解答 解:A.硝酸銀溶液跟銅反應的離子反應為Cu+2Ag+═Cu2++2Ag,故A錯誤;
B.鐵粉跟稀鹽酸反應的離子反應為Fe+2H+═Fe2++H2↑,故B錯誤;
C.硫酸和氫氧化鋇反應的離子反應為2H++SO42-+Ba2++2OH-═2H2O+BaSO4↓,故C錯誤;
D.用小蘇打治療胃酸過多的離子反應為HCO3-+H+═CO2↑+H2O,故D正確;
故選D.
點評 本題考查離子反應方程式的書寫,為高頻考點,把握發生的反應及離子反應的書寫方法為解答的關鍵,側重分析與應用能力的考查,注意離子反應中保留化學式的物質,題目難度不大.


 浙江之星學業水平測試系列答案
浙江之星學業水平測試系列答案 高效智能課時作業系列答案
高效智能課時作業系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 吸氧腐蝕時正極放出O2 | |
| B. | 析氫腐蝕時正極放出H2 | |
| C. | 析氫腐蝕比吸氧腐蝕普遍 | |
| D. | 析氫腐蝕與吸氧腐蝕的負極反應都是Fe-3e-=Fe3+ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
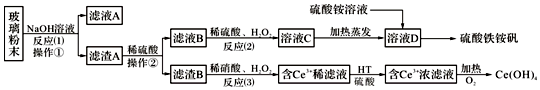
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com