
分析 (1)碳的燃燒熱△H1=a kJ•mol-1,其熱化學方程式為C(s)+O2(g)=CO2(g)△H1=a kJ•mol-1①
S(s)+2K(s)═K2S(s)△H2=b kJ•mol-1②
2K(s)+N2(g)+3O2(g)═2KNO3(s)△H3=c kJ•mol-1③
將方程式3①+②-③得S(s)+2KNO3(s)+3C(s)═K2S(s)+N2(g)+3CO2(g),其反應熱進行相應的改變,據此計算反應熱;
(2)依據蓋斯定律和已知熱化學方程式求出Cl2(g)+PCl3(g)=PCl5(g)的反應熱,再依據焓變=反應物鍵能之和-生成物鍵能之和計算分析;
(3)已知:①I2(g)+H2(g)?2HI(g)△H=-9.48kJ•mol-1;②I2(s)+H2(g)?2HI(g)△H=+26.48kJ•mol-1,利用蓋斯定律將①-②可得I2(g)=I2(s)△H=-9.48kJ•mol-1-26.48kJ•mol-1=-35.96kJ•mol-1;
(4)根據蓋斯定律利用鋁熱反應為放熱反應來判斷.
解答 解:(1)碳的燃燒熱△H1=a kJ•mol-1,其熱化學方程式為C(s)+O2(g)=CO2(g)△H1=a kJ•mol-1①
S(s)+2K(s)═K2S(s)△H2=b kJ•mol-1②
2K(s)+N2(g)+3O2(g)═2KNO3(s)△H3=c kJ•mol-1③
將方程式3①+②-③得S(s)+2KNO3(s)+3C(s)═K2S(s)+N2(g)+3CO2(g),則△H=x kJ•mol-1=(3a+b-c)kJ•mol-1,所以x=3a+b-c,
故答案為:S(s)+2KNO3(s)+3C(s)═K2S(s)+N2(g)+3CO2(g)△H=(3a+b-c)kJ/mol;
(2)已知:①P4(g)+6Cl2(g)=4PCl3(g)△H=a kJ?mol-1;
②P4(g)+10Cl2(g)=4PCl5(g)△H=b kJ?mol-1;
利用“蓋斯定律”,(②-①)×$\frac{1}{4}$得:Cl2(g)+PCl3(g)=PCl5(g)△H=$\frac{b-a}{4}$KJ•mol-1,
由Cl2(g)+PCl3(g)=PCl5(g)△H=$\frac{b-a}{4}$KJ•mol-1 可得E(Cl-Cl)+3×1.2c-5c=$\frac{b-a}{4}$,
因此可得:E(Cl-Cl)=$\frac{b-a+5.6c}{4}$kJ•mol-1=1.4c+0.25b-0.25akJ•mol-1;
故答案為:1.4c+0.25b-0.25a;
(3)已知:①I2(g)+H2(g)?2HI(g)△H=-9.48kJ•mol-1;②I2(s)+H2(g)?2HI(g)△H=+26.48kJ•mol-1,利用蓋斯定律將①-②可得I2(g)=I2(s)△H=-9.48kJ•mol-1-26.48kJ•mol-1=-35.96kJ•mol-1,所以1mol固態碘轉化為氣態碘需吸收35.96kJ的能量;
故答案為:吸收;35.96;
(4)4Al(s)+3O2(g)═2Al2O3(s)△H1 ①
4Fe(s)+3O2(g)═2Fe2O3(s)△H2 ②
由蓋斯定律①-②,得:4Al(s)+2Fe2O3═2Al2O3(s)+4Fe(s)△H1 -△H2,
鋁熱反應為放熱反應,即△H1 -△H2<0,所以△H1<△H2,
故答案為:<.
點評 本題考查蓋斯定律的應用,側重考查學生分析計算能力,明確目標方程式與已知方程式的關系是解本題關鍵,注意方程式可以進行加減,題目難度中等.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
| A. | Al | B. | Mg | ||
| C. | Na | D. | 三者產生的氫氣一樣多 |
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河南省高二上第一次月考化學卷(解析版) 題型:選擇題
下列變化中,屬于吸熱反應的是( )
①液態水的 汽化 ②將膽礬加熱變為白色粉末
汽化 ②將膽礬加熱變為白色粉末
③濃硫酸稀釋 ④KCl03分解制氧氣
⑤生石灰跟水反應生成熟石灰
⑥CaCO3高溫分解⑦CO2+C 2CO
2CO
⑧Ba(OH)2·8H2O與固體NH4Cl混合
⑨C(s)+H2O(g) CO(g)+H2(g)⑩Al與鹽酸反應
CO(g)+H2(g)⑩Al與鹽酸反應
A. ②③④⑤⑥⑦⑧⑨ B.②④⑥⑦⑧⑨ C.②④⑥⑧ D.②③④⑧⑨
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 131I是一種新發現的元素 | |
| B. | 我們平常食用的加碘鹽就是含有碘單質的食鹽 | |
| C. | 鹵素F、Cl、Br、I中,I的電負性和第一電離能都最小 | |
| D. | 碘單質易升華是由于碘原子半徑大,共價鍵鍵能小 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
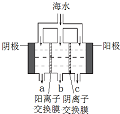 海洋是豐富的資源寶庫,通過海水的綜合利用可獲得許多物質供人類使用.
海洋是豐富的資源寶庫,通過海水的綜合利用可獲得許多物質供人類使用.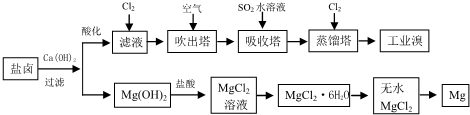
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 若在海輪外殼上附著一些銅塊,則可以減緩海輪外殼的腐蝕 | |
| B. | 一定條件下反應N2+3H22?NH3達到平衡時,3v正(H2)=2v逆(NH3) | |
| C. | 酸堿質子理論認為,凡能給出質子(H+) 的物質都是酸,凡能接受質子的物質都是堿.根據這一理論,Al(OH)3、NaHCO3都是兩性物質 | |
| D. | 對于乙酸與乙醇的酯化反應(△H<0),加入少量濃硫酸并加熱,該反應的反應速率和平衡常數均增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | KOH溶液與AlCl3溶液 | B. | NaAlO2溶液與鹽酸 | ||
| C. | NaHCO3溶液與鹽酸 | D. | Na2CO3溶液與鹽酸 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 某學習小組依據SO2具有還原性,推測SO2能被Cl2氧化生成SO2Cl2.
某學習小組依據SO2具有還原性,推測SO2能被Cl2氧化生成SO2Cl2.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
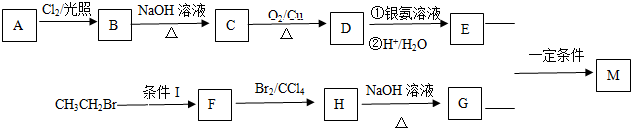
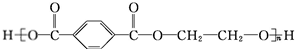 .
.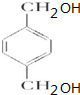 +O2$→_{△}^{Cu}$
+O2$→_{△}^{Cu}$ +2H2O.
+2H2O.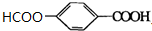 (寫出所有可能的結構簡式)
(寫出所有可能的結構簡式)查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com