

分析 由流程圖可知,海水可用于制取純堿,也可用于制備金屬鎂,制備純堿時,海水經蒸發、提純得到精鹽,溶于水在水中先通入氨氣,然后通入二氧化碳氣體,可生成溶解度較小的碳酸氫鈉,經過濾、洗滌和加熱和得到碳酸鈉固體;
海水中含有氯化鎂,加入石灰水,可生成氫氧化鎂沉淀,過濾后在沉淀中加入鹽酸可生成氯化鎂,經蒸發、結晶和脫水后可得氯化鎂,電解熔融的氯化鎂可得金屬鎂,
(1)從溶液中獲得晶體,可經蒸發、冷卻結晶等操作;
(2)制備純堿,由于氨氣易溶于水,而二氧化碳微溶,應在飽和氯化鈉溶液中先通入氨氣,然后再通入二氧化碳氣體,發生NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl;
(3)從鹽類水解的角度分析;
(4)①根據AgCl的Ksp計算c(Ag+),然后計算c(CrO42;
②滴定時先生成AgCl沉淀,當AgCl全部沉淀時,再生成Ag2CrO4磚紅色沉淀且半分鐘內不再消失,此時可說明達到滴定終點,根據硝酸銀的物質的量計算質量分數;
③a.盛放AgNO3溶液的滴定管水洗后未用標準液潤洗,導致硝酸銀溶液濃度偏低;
b.滴定管滴定前尖嘴部分有氣泡,滴定后消失,導致所用體積偏大;
c.滴定前仰視讀數,滴定后俯視讀數,導致體積偏小.
解答 解:(1)實驗室提純粗鹽的實驗操作方法為:取樣、溶解、過濾、蒸發、冷卻結晶等操作,故答案為:過濾;蒸發(或蒸發結晶);
(2)制備純堿,由于氨氣易溶于水,而二氧化碳微溶,應在飽和氯化鈉溶液中先通入氨氣,然后在通入二氧化碳氣體,發生NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl,
如用題給圖裝置制備,由于氨氣易溶于水,為防止倒吸,則a通入氨氣,儀器c為干燥管,
故答案為:CO2;NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl;干燥管;NH3;
(3)如果直接在空氣中加熱MgCl2•6H2O則Mg2+會水解的生成Mg(OH)Cl和HCl,通入HCl可以抑制其水解,故答案為:在HCl氣流中加熱;
(4)①Cl-恰好沉淀完全即溶液中殘余c(Cl-)=1.0×10-5 mol•L-1,c(Ag+)=$\frac{Ksp}{c(C{l}^{-})}$=$\frac{2×1{0}^{-10}}{1.0×1{0}^{-5}}$=2.0×10-5mol/L,
則此時溶液中的c(CrO42-)=$\frac{Ksp}{{c}^{2}(A{g}^{+})}$=$\frac{1.12×1{0}^{-12}}{(2.0×1{0}^{-5})^{2}}$=2.8×10-3;
故答案為:2.8×10-3;
②析出沉淀時,AgCl溶液中c(Ag+)=$\frac{{K}_{sp}(AgCl)}{c(C{l}^{-})}$=$\frac{1.56×1{0}^{-10}}{0.01}$mol/L=1.56×10-8mol/L,
Ag2CrO4溶液中c(Ag+)=$\sqrt{\frac{{K}_{sp}(A{g}_{2}Cr{O}_{4})}{c({Cr{O}_{4}}^{2-})}}$=$\sqrt{\frac{9.0×1{0}^{-12}}{0.01}}$mol/L=3×10-5,
則滴定時先生成AgCl沉淀,當AgCl全部沉淀時,再生成Ag2CrO4磚紅色沉淀且半分鐘內不再消失,此時可說明達到滴定終點,由于硝酸銀見光易分解,應放在棕色滴定管內,
若此時消耗了AgNO3標準溶液v mL,則n(AgNO3)=cv×10-3mol,可知n(Cl-)=cv×10-3mol,
因配成100mL溶液,取出20mL注入錐形瓶中,則原樣品中含有n(Cl-)=5cv×10-3mol,
則質量分數為$\frac{cv×1{0}^{-3}×5×35.5}{a}×100%$,
故答案為:防止硝酸銀見光分解;磚紅色沉淀且在半分鐘內不再消失;$\frac{cv×1{0}^{-3}×5×35.5}{a}×100%$;
③a.盛放AgNO3溶液的滴定管水洗后未用標準液潤洗,導致硝酸銀溶液濃度偏低,所用體積偏大,則測定及結果偏高,故a錯誤;
b.滴定管滴定前尖嘴部分有氣泡,滴定后消失,導致所用體積偏大,則測定及結果偏高,故b錯誤;
c.滴定前仰視讀數,滴定后俯視讀數,導致體積偏小,則測定結果偏小,故c正確.
故答案為:c.
點評 本題主要考查了粗鹽的提純、候氏制堿、海水中提取Mg的原理以及含量的測定,為高頻考點,側重于學生的分析能力和實驗能力的考查,注意把握實驗的原理和操作方法,難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | 同濃度、同體積的強酸與強堿溶液混合后,溶液的pH=7 | |
| B. | 在含有BaSO4沉淀的溶液中加人Na2SO4固體,c(Ba2+)增大 | |
| C. | 含1molKOH的溶液與lmolCO2完全反應后,溶液中c(K+ )=c (HCO3- ) | |
| D. | 改變條件使醋酸溶液中的醋酸根離子濃度增大,溶液的pH值可能減小也可能增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1mol苯分子中含有雙鍵數 | |
| B. | 1mol CaC2固體中含陰離子總數 | |
| C. | 1L 1mol/L CH3COOH溶液中所含分子總數 | |
| D. | 1mol Cl2參加化學反應獲得的電子數 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 實驗操作及現象 | 現象的解釋 | |
| A | 將一片鋁箔置于酒精燈外焰上灼燒,鋁箔熔化但不滴落 | 單質鋁的熔點特別高 |
| B | 用玻璃尖嘴導管導出氫氣,點燃,觀察到火焰呈黃色 | 普通玻璃中含有鈉元素 |
| C | 往水中加入Na2O2固體,滴入酚酞呈紅色,振蕩,紅色褪去 | 產生了堿性物質,且Na2O2具有漂白性 |
| D | 向過量的苯酚濃溶液中滴加少許飽和溴水,振蕩,未觀察到白色沉淀產生 | 三溴苯酚溶解在過量的苯酚中 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 推廣使用聚二氧化碳可降解塑料,能減少白色污染 | |
| B. | 通常所說的三大有機合成材料是指塑料、合成纖維、合成橡膠 | |
| C. | 實驗“煤改氣”“煤改電”等清潔燃料改造工程,有利于保護環境 | |
| D. | 夏天雷雨過后感覺到空氣清新是因為空氣中產生了少量的二氧化氮 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 做衣服的棉和麻均與淀粉互為同分異構體 | |
| B. | 煎炸食物的花生油和牛油都是可皂化的飽和酯類 | |
| C. | 磨豆漿的大豆富含蛋白質,豆漿煮沸后蛋白質變成了氨基酸 | |
| D. | 施肥時,草木灰(有效成分為K2CO3)和NH4Cl混合使用,會產生氨氣降低肥效 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向硫酸鋁溶液中滴加過量的氨水:Al3++4OH-═AlO2-+2H2O | |
| B. | 金屬銅與濃硝酸反應:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O | |
| C. | 實驗室制備氫氧化鐵膠體:Fe3++3H2O═Fe(OH)3(膠體)+3H+ | |
| D. | 向苯酚鈉溶液中通入少量的二氧化碳氣體:2C6H5ONa+CO2+H2O═2C6H6O+Na2CO3 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
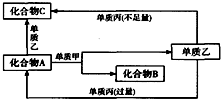 A、B、C都是由兩種元素組成的無機物,它們和單質甲、乙、丙在如圖所示的轉化關系(轉化過程都不需要使用催化劑).
A、B、C都是由兩種元素組成的無機物,它們和單質甲、乙、丙在如圖所示的轉化關系(轉化過程都不需要使用催化劑).查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com