
| 實驗I | 實驗II | 實驗III | |
| 反應溫度/℃ | 800 | 800 | 850 |
| c( A)起始/mol•L-1 | 1 | 2 | 1 |
| c( A)平衡/mol•L-1 | 0.5 | 1 | 0.85 |
| 放出的熱量/kJ | a | b | c |
| A. | 化學平衡常數實驗III的小于實驗I的 | |
| B. | 實驗放出的熱量關系為b>2a | |
| C. | 實驗III 在30min達到平衡,用A表示此段時間的平均反應速率v (A)為0.005mol•L-1•min-1 | |
| D. | 當容器內氣體密度不隨時間而變化時上述反應已達平衡 |
分析 A.該反應為放熱反應,升高溫度,平衡逆向移動;
B.根據反應兩邊氣體的體積相等,壓強不影響化學平衡,實驗Ⅰ和實驗Ⅱ為等效平衡進行分析;
C.根據實驗Ⅲ中的數據計算出A的反應速率;
D.根據B是固體,反應兩邊質量不相等,容器的容積固定進行判斷.
解答 解:A.該反應為放熱反應,升高溫度,平衡逆向移動,平衡常數減小,已知實驗III的溫度高平衡常數小,即化學平衡常數實驗III的小于實驗I的,故A正確;
B.實驗II中氣體物質的量是實驗I中2倍,則壓強是實驗I的2倍,反應兩邊氣體的體積相等,壓強不影響化學平衡,實驗Ⅰ和實驗Ⅱ為等效平衡,反應消耗的A的物質的量,實驗Ⅱ是實驗Ⅰ的2倍,放出的熱量b=2a,故B錯誤;
C.根據A項的計算,A的濃度變化是0.15mol/L,A的平均反應速率為:$\frac{0.15mol/L}{30min}$=0.005mol•L-1•min-1,故C正確;
D.由于反應方程式中B是固體,反應兩邊氣體的質量不相等,而容器的容積固定,根據ρ=$\frac{m}{V}$,V是定值,密度不變,說明混合氣體的質量不變,正逆反應速率相等,達到了平衡狀態,故D正確.
故選:B.
點評 本題考查了化學平衡的計算,涉及了化學平衡常數的計算、化學平衡狀態的判斷、化學反應速率的計算等知識,本題難度中等,試題有利于培養學生的分析、理解能力及化學計算能力.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
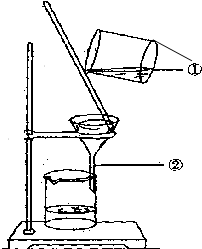 如圖為某學生進行粗鹽提純實驗中過濾操作的示意圖,試回答:
如圖為某學生進行粗鹽提純實驗中過濾操作的示意圖,試回答:查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
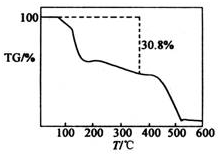 硫酸錳銨[(NH4)2SO4•MnSO4•nH2O]是淺粉色晶體,易溶于水,在農業上用作微量元素肥料.實驗室由MnO2制備硫酸錳銨的實驗步驟如下:
硫酸錳銨[(NH4)2SO4•MnSO4•nH2O]是淺粉色晶體,易溶于水,在農業上用作微量元素肥料.實驗室由MnO2制備硫酸錳銨的實驗步驟如下:查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在化學反應過程中,發生物質變化的同時一定發生能量變化 | |
| B. | 破壞生成物全部化學鍵所需要的能量大于破壞反應物全部化學鍵所需要的能量時,反應為吸熱反應 | |
| C. | 反應產物的總焓大于反應物的總焓時,反應吸熱,△H>0 | |
| D. | 熱化學方程式中反應熱數值的大小與化學方程式的計量數成比例 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 升高溫度能加快反應速率的主要原因,是增加了反應物分子中活化分子的百分數 | |
| B. | 正反應是吸熱反應,達到平衡時,升高溫度,v正增大,v逆減小,所以平衡向正反應方向移動 | |
| C. | 一定條件下增大反應物的量,一定會加快反應速率 | |
| D. | 對于任何一個化學反應,用其中任何一種反應物濃度的減小來表示化學反應速率,都是相同的數值 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
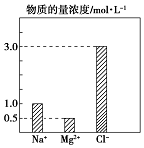 某100mL溶液中含有的部分離子濃度大小如圖所示,該溶液可能還含有Fe3+、Ba2+、H+、SO42-、CO32-.為了進一步確認,對該溶液進行實驗檢測:
某100mL溶液中含有的部分離子濃度大小如圖所示,該溶液可能還含有Fe3+、Ba2+、H+、SO42-、CO32-.為了進一步確認,對該溶液進行實驗檢測:| 實驗操作與現象 | 實驗結論 | 判斷理由 | |
| 步驟一 | 仔細觀察坐標圖 | 肯定無 CO32- | 肯定無該離子的理由碳酸根離子和鎂離子之間會反應 |
| 步驟二 | 該溶液呈無色、透明、均一狀態 | 肯定無 Fe3+ | 肯定無該離子的理由該離子為黃色 |
| 步驟三 | 加入足量BaCl2溶液,生成23.3g白色沉淀,再加稀硝酸,沉淀不消失 | 肯定有SO42-、H+;肯定無Ba2+ | 肯定有H+的理由電荷守恒 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com