
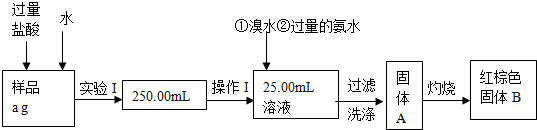

分析 (1)根據配制一定物質的量濃度的溶液所需要的儀器有:量筒、膠頭滴管、燒杯、玻璃棒、一定規格的容量瓶;
(2)根據Br2具有氧化性,能氧化Fe2+寫出反應的離子方程式;
(3)紅棕色固體( Fe2O3)中的鐵就是樣品中鐵,根據質量分數的公式求出鐵元素的質量分數;
(4)①溶解樣品若用鹽酸,用高錳酸鉀若用滴定時會氧化氯離子,影響實驗測定結果;
②某氯化鐵與氯化亞鐵的混合物,現要測定其中鐵元素的質量分數,加入鐵做還原劑和過量的硫酸反應生成亞鐵離子,會增加鐵元素的量對測定結果產生誤差;
③酸性條件下高錳酸根離子將亞鐵離子氧化成鐵離子,同時被還原生成錳離子;
④尖嘴部位有氣泡,滴定后氣泡消失,導致消耗的標準液體積偏大,測定的鐵元素的量偏高.
解答 解:(1)因配制一定物質的量濃度的溶液所需要的儀器有:量筒、膠頭滴管、燒杯、玻璃棒、一定規格的容量瓶,所以還缺少250mL的容量瓶,
故答案為:250mL容量瓶;
(2)因Br2具有氧化性,能氧化Fe2+,反應的離子方程式為:2Fe2++Br2=2Fe3++2Br-,
故答案為:2Fe2++Br2=2Fe3++2Br-;
(3)紅棕色固體中的鐵就是樣品中鐵,根據鐵元素質量守恒,mgFe2O3中鐵元素的質量為mg×$\frac{112}{160}$,則250mL配制的溶液中含有鐵元素的質量為:mg×$\frac{112}{160}$×$\frac{250mL}{25mL}$=
7mg,
則樣品中鐵元素的質量分數是:$\frac{7mg}{ag}$×100%=$\frac{7m}{a}$×100%,
故答案為:$\frac{7m}{a}$×100%;
(4)①高錳酸鉀具有強氧化性,加入鹽酸,溶液中的氯離子會被氧化,多消耗高錳酸鉀,產生實驗測定誤差,所以溶解樣品不能用鹽酸,應該用硫酸,
故答案為:鹽酸中的Cl-對KMnO4溶液滴定有干擾;
②還原劑不能用鐵,因為有貼分會和過量硫酸反應生成硫酸亞鐵,再用高錳酸鉀滴定,多消耗氧化劑產生誤差,干擾原混合物的鐵元素的測定,
故答案為:Fe與硫酸反應生成Fe2+影響鐵元素質量分數的測定;
③酸性條件下用KMnO4滴定,亞鐵離子被氧化成鐵離子,反應的離子方程式為:5Fe2++MnO4-+8H+=Mn2++5Fe3++4H2O,
故答案為:5Fe2++MnO4-+8H+=Mn2++5Fe3++4H2O;
④用滴定管裝KMnO4溶液后如尖嘴部位有氣泡,滴定后氣泡消失,導致計算出消耗的酸性高錳酸鉀溶液的體積偏大,所測得混合中Fe元素的物質的量偏大,則計算出的鐵元素的含量偏大,
故答案為:偏大.
點評 本題考查了探究物質組成、測量物質含量的方法,題目難度中等,明確實驗目的及實驗原理為解答關鍵,注意配制的溶液與實驗中所取溶液體積關系,為易錯點,試題培養了學生的化學實驗能力.


科目:高中化學 來源: 題型:選擇題
| A. | NaOH | B. | H2SO4 | C. | CH3COONa | D. | KCl |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Fe-3e一═Fe3+ | B. | Fe2+十20H-═Fe(OH)2 | ||
| C. | 2H20+02+4e-═40H- | D. | 4Fe(OH)2+2H20+02═4Fe(OH)3 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向碳酸氫銨溶液中加入足量的氫氧化鈉溶液:HCO3-+OH-═CO32-+H2O | |
| B. | 向Ba(OH)2溶液中滴加NaHSO4溶液至恰好為中性:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| C. | 用酸化的高錳酸鉀溶液氧化雙氧水:2MnO4-+6H++5H2O2═2Mn2++5O2↑+8H2O | |
| D. | Ca(ClO)2溶液中通入過量的二氧化硫氣體:ClO-+SO2+H2O═HClO+HSO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 主要是用來吸收或滴加少量試劑,以及吸取上層清液,分離沉淀 | |
| B. | 進行滴加的時候,膠頭滴管要保持垂直在容器正上方 | |
| C. | 取液體時,先將膠頭滴管伸入試劑瓶中,用手指捏緊滴管的膠頭再放開手指 | |
| D. | 專用的膠頭滴管在使用完之后,就一定要放回原試劑中 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 某物質既能溶于鹽酸,又能溶于NaOH溶液,則該物質一定是Al2O3 | |
| B. | 某氣體只含C、H兩種元素,且質量之比為6:1,則該氣體一定為純凈物 | |
| C. | SO2通入品紅溶液中,溶液褪色,則SO2通入紫色石蕊試液中,溶液也褪色 | |
| D. | 濃硝酸在光照條件下變黃,說明濃硝酸不穩定,生成的有色產物能溶于濃硝酸 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com