
| 編號 | ① | ② | ③ | ④ |
| 稀硝酸體積/ml | 100mL | 200mL | 300mL | 400mL |
| 剩余金屬/g | 18.0g | 9.6g | 0 | 0 |
| NO體積/L | 2.24L | 4.48L | 6.7L | V |
分析 由表中數據可知,實驗①②都有金屬剩余,則溶液中不可能含有硝酸鐵,溶液中金屬離子為+2價,在實驗①的基礎上加入100mL硝酸,參加反應的金屬的質量為18g-9.6g=8.4g,
生成NO的體積為4480mL-2240mL=2240mL,NO物質的量為0.1mol,
根據電子轉移守恒可知,參加反應金屬的物質的量為:$\frac{0.1mol×(5-2)}{2}$=0.15mol,
參加反應金屬的平均摩爾質量為:$\frac{8.4g}{0.15mol}$=56g/mol,
故該過程只有Fe參加反應,故實驗①只有Fe參與反應,
根據NO的體積結合方程式計算硝酸的物質的量、參加反應Fe的物質的量,
根據c=$\frac{n}{V}$計算硝酸的物質的量濃度,根據m=nM計算①中參加反應Fe的質量;
在實驗②的基礎上加入100mL硝酸,參加反應的金屬的質量為9.6g,生成NO的體積為6720mL-4480mL=2240mL,NO物質的量為0.1mol,
若該過程只有Cu參加反應,根據電子轉移守恒,
則Cu的物質的量=$\frac{0.1mol×(5-2)}{2}$=0.15mol,Cu的質量=0.15mol×64g/mol=9.6g,等于參加反應金屬的質量,
故該過程只有Cu反應,且Cu恰好完全反應,
故加入200mL硝酸時,Fe恰好反應生成硝酸亞鐵,在實驗③的基礎上再加入100mL硝酸,為硝酸與溶液中亞鐵離子反應生成NO,
根據亞鐵離子的物質的量,利用電子轉移守恒計算該階段生成NO的物質的量,再根據V=nVm計算該階段生成NO的體積,進而計算V的值;
每份金屬混合物為①中溶解的Fe與實驗①剩余的金屬的質量之和.
解答 解:由表中數據可知,實驗①②都有金屬剩余,則溶液中不可能含有硝酸鐵,溶液中金屬離子為+2價,在實驗①的基礎上加入100mL硝酸,參加反應的金屬的質量為18g-9.6g=8.4g,
生成NO的體積為4480mL-2240mL=2240mL,NO物質的量為0.1mol,
根據電子轉移守恒可知,參加反應金屬的物質的量為:$\frac{0.1mol×(5-2)}{2}$=0.15mol,
參加反應金屬的平均摩爾質量為:$\frac{8.4g}{0.15mol}$=56g/mol,
故該過程只有Fe參加反應,故實驗①只有Fe參與反應;
在實驗②的基礎上加入100mL硝酸,參加反應的金屬的質量為9.6g,生成NO的體積為6720mL-4480mL=2240mL,NO物質的量為0.1mol,
若該過程只有Cu參加反應,根據電子轉移守恒,
則Cu的物質的量=$\frac{0.1mol×(5-2)}{2}$=0.15mol,Cu的質量=0.15mol×64g/mol=9.6g,等于參加反應金屬的質量,
故該過程只有Cu反應,且Cu恰好完全反應,
故加入200mL硝酸時,Fe恰好反應生成硝酸亞鐵,在實驗③的基礎上再加入100mL硝酸,為硝酸與溶液中亞鐵離子反應生成NO,
(1)由上述分析可知,實驗①發生反應3Fe+8HNO3═3Fe(NO3)2+2NO↑+4H2O,生成NO的物質的量為:$\frac{2.24L}{22.4L/mol}$=0.1mol,
根據方程式可知,參加反應的硝酸的物質的量為0.1mol×4=0.4mol,
故硝酸的物質的量濃度為:$\frac{0.4mol}{0.1L}$=4mol/L,
答:硝酸的濃度為4mol/L;
(2)由上述分析可知,實驗①發生反應3Fe+8HNO3═3Fe(NO3)2+2NO↑+4H2O,生成NO的物質的量為0.1mol,
根據方程式可知,參加反應的Fe的物質的量為0.1mol×$\frac{3}{2}$=0.15mol,
故參加反應Fe的質量=0.15mol×56g/mol=8.4g,即①中溶解了8.4gFe,
故每份溶液中含有金屬的質量為:8.4g+18g=26.4g,
答:每份金屬混合物的質量為26.4g;
(3)由上述分析可知,實驗②中Fe與硝酸恰好反應生成硝酸亞鐵,生成NO的物質的量=$\frac{4.48L}{22.4L/mol}$=0.2mol,
由3Fe+8HNO3═3Fe(NO3)2+2NO↑+4H2O可知,溶液中亞鐵離子的物質的量為0.3mol,在實驗③的基礎上再加入100mL硝酸,為硝酸與溶液中亞鐵離子反應生成NO,
根據電子轉移守恒可知,生成NO的物質的量=$\frac{0.3mol×(3-2)}{5-2}$=0.1mol,
故生成NO的體積為:0.1mol×22.4L/mol=2.24L=2240mL,
故V=6720+2240=8960,
答:實驗④中V的值為8960.
點評 本題考查混合物的有關計算、化學方程式的計算,題目難度較大,根據表中數據判斷各階段發生的反應是關鍵,側重對學生綜合能力的考查,過程復雜、計算量較大,試題充分考查了學生的分析能力及化學計算能力.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
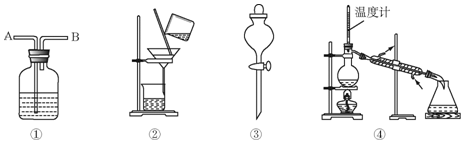
| 選項 | 物質 | 試劑 | 裝置 |
| A | C2H6(C2H4) | ① | ① |
| B | 苯(苯酚) | ⑥ | ② |
| C | 苯(苯甲酸) | ⑤ | ④ |
| D | 甲苯(二甲苯) | ③ | ③ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | K+、MnO4-、Cl-、SO42- | B. | Na+、AlO2-、Cl-、SO42- | ||
| C. | SO42-、Fe3+、HCO3-、Ba2+ | D. | Mg2+、NO3-、NH4+、SO42- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 化學反應及對離子方程式 | 評價 |
| A | 金屬鈉加入滴有酚酞的水中:Na+H2O═Na++OH-+H2↑ | 正確 |
| B | 等體積等物質的量濃度的AlCl3、Ba(OH)2、HCl溶液混合:Al3+3H+6OH-═Al(OH)3↓+3H2O | 正確 |
| C | 向硅酸鈉溶液中通入過量CO2:SiO32-+2H2O+2CO2═H2SiO3↓+2HC3-O | 錯誤,CO2過量溶液應該變澄清 |
| D | 向氯化鈉鋁溶液中加入足量氨水溶液:Al3++4NH3•H2O═AlO2+2H2O+4NH4+ | 正確 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
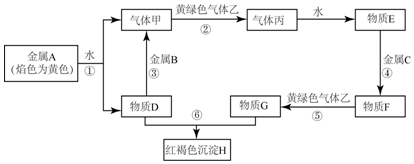
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①②③ | B. | ①③④ | C. | ①②④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
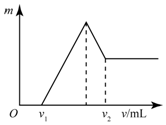 (1)為了檢驗某含有NaHCO3雜質的Na2CO3樣品的純度,現將100g樣品加熱使其質量不再變化,其質量變為96.9%,則該樣品的純度(質量分數)是91.6%
(1)為了檢驗某含有NaHCO3雜質的Na2CO3樣品的純度,現將100g樣品加熱使其質量不再變化,其質量變為96.9%,則該樣品的純度(質量分數)是91.6%查看答案和解析>>
科目:高中化學 來源: 題型:解答題
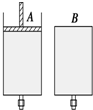 如圖所示,有兩只密閉容器A和B,A容器有一個移動的活塞能使容器內保持恒壓,B容器能保持恒容.起始時向這兩只容器中分別充入等量的體積比為2:1的SO2與O2的混合氣體,并使A和B容積相等(如圖).在保持400℃的條件下使之發生如下反應:2SO2(g)+O2(g)$?_{△}^{催化劑}$2SO3(g),填寫下列空格.
如圖所示,有兩只密閉容器A和B,A容器有一個移動的活塞能使容器內保持恒壓,B容器能保持恒容.起始時向這兩只容器中分別充入等量的體積比為2:1的SO2與O2的混合氣體,并使A和B容積相等(如圖).在保持400℃的條件下使之發生如下反應:2SO2(g)+O2(g)$?_{△}^{催化劑}$2SO3(g),填寫下列空格.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 被提純的物質 | 雜質 | 除雜試劑 | |
| A | H2S | H2O | 無水CuSO4 |
| B | NH3 | H2O | 無水CuCl2 |
| C | SO2 | HCl | 飽和食鹽水、濃硫酸 |
| D | CO2 | HCl | 飽和NaHCO3溶液、濃硫酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com