
| 時間(s) C(mol/L) | 0 | 20 | 40 | 60 | 80 | 100 |
| C(N2O4) | 0.20 | a | 0.10 | c | d | e |
| C(NO2) | 0.00 | 0.12 | b | 0.22 | 0.22 | 0.22 |
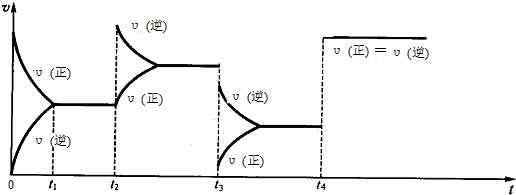
分析 (1)t2時正反應速率瞬間不變,逆反應速率增大,然后逆反應速率逐漸減小,正反應速率逐漸增大,直至重新達到平衡,說明t2時加入了加入N2O4;
t3時正逆反應速率瞬間同時減小,且逆反應速率減小的幅度小于正反應速率,即v(正)<v(逆),平衡向著逆向移動,正反應為氣體體積減小的放熱反應,應是降低溫度;
t4時刻正逆反應速率同時增大,且相等,改變的條件不影響化學平衡,則說明使用了催化劑;
(2)40s時轉化的N2O4為0.2mol/L-0.1mol/L=0.1mol/L,NO2的產率等于N2O4的轉化率;
(3)20s時,NO2濃度為0.12mol/L,則△c(N2O4)=$\frac{1}{2}$×0.12mol/L=0.06mol/L,20sN2O4的濃度=N2O4的起始濃度-△c(N2O4),根據v=$\frac{△c}{△t}$計算0~20s內N2O4的平均反應速率;
(4)平衡時NO2濃度為0.22mol/L,則c(N2O4)=0.2mol/L-$\frac{1}{2}$×0.22mol/L=0.09mol/L,再根據K=$\frac{{c}^{2}(N{O}_{2})}{c({N}_{2}{O}_{4})}$計算平衡常數;
(5)K值越大,說明正反應進行的程度越大;
(6)已知:①CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ/mol
②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H2=-1160kJ/mol
根據蓋斯定律,(①+②)÷2可得:CH4(g)+2NO2(g)=CO2(g)+2H2O(g)+N2(g).
解答 解:(1)t2時正反應速率瞬間不變,逆反應速率增大,然后逆反應速率逐漸減小,正反應速率逐漸增大,直至重新達到平衡,說明t2時加入了加入N2O4;
t3時正逆反應速率瞬間同時減小,且逆反應速率減小的幅度小于正反應速率,即v(正)<v(逆),平衡向著逆向移動,正反應為氣體體積減小的放熱反應,應是降低溫度;
t4時刻正逆反應速率同時增大,且相等,改變的條件不影響化學平衡,則說明使用了催化劑,
故答案為:增大生成物N2O4的濃度;降低壓強;加入催化劑;
(2)40s時轉化的N2O4為0.2mol/L-0.1mol/L=0.1mol/L,NO2的產率等于N2O4的轉化率,則NO2的產率為$\frac{0.1mol/L}{0.2mol/L}$×100%=50%,
故答案為:50%;
(3)20s時,NO2濃度為0.12mol/L,則△c(N2O4)=$\frac{1}{2}$×0.12mol/L=0.06mol/L,20sN2O4的濃度=0.2mol/L-0.06mol/L=0.14mol/L,0~20s內N2O4的平均反應速率為$\frac{0.06mol/L}{20s}$=0.003mol/(L.s),
故答案為:0.14;0.003mol/(L.s);
(4)平衡時NO2濃度為0.22mol/L,則c(N2O4)=0.2mol/L-$\frac{1}{2}$×0.22mol/L=0.09mol/L,則平衡常數K=$\frac{{c}^{2}(N{O}_{2})}{c({N}_{2}{O}_{4})}$=$\frac{0.2{2}^{2}}{0.09}$=0.54,
故答案為:0.54;
(5)K值越大,說明正反應進行的程度越大,則N2O4的轉化率越高、NO2的產量越大,N2O4與NO2的濃度之比越小,
故選:ABD;
(6)已知:①CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ/mol
②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H2=-1160kJ/mol
根據蓋斯定律,(①+②)÷2可得:CH4(g)+2NO2(g)=CO2(g)+2H2O(g)+N2(g)△H=-867 kJ/mol,
故答案為:CH4(g)+2NO2(g)=CO2(g)+2H2O(g)+N2(g)△H=-867 kJ/mol.
點評 本題考查化學平衡計算與影響因素、化學平衡圖象、反應速率與平衡常數、蓋斯定律應用等,側重考查學生讀圖提取信息能力與知識遷移運用能力,難度中等.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
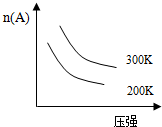
| A. | 3A(g)+B(g)?2C(g);△H<0 | B. | A(g)+3B(s)+2C(g)?3D(g);△H<0 | ||
| C. | C(s)+D(g)?A(g)+B(g)△H>0 | D. | 2C(g)?2A(g)+B(g)△H>0 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 等于p% | B. | 大于p% | C. | 小于p% | D. | 無法判斷 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | c(CH3COO-)=c(Cl-)=c(H+)>c(CH3COOH) | B. | c(CH3COO-)=c(Cl-)>c(CH3COOH)>c(H+) | ||
| C. | c(CH3COO-)>c(Cl-)>c(H+)>c(CH3COOH) | D. | c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.1 mol/L Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+c(H2CO3) | |
| B. | 常溫下,NH4Cl和NH3•H2O混合溶液的PH=7:c(NH4+ )=c(Cl-) | |
| C. | 向醋酸溶液中加入適量醋酸鈉,得到的堿性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | |
| D. | 常溫下,向硝酸鉀溶液中滴加稀鹽酸得到的pH=5的混合溶液:c(K+)>c(NO3-) |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
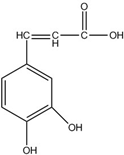
| A. | 分子式為C9H5O4 | |
| B. | 1mol該有機物最多可與3mol氫氣發生加成反應 | |
| C. | 與溴水既能發生取代反應,又能發生加成反應 | |
| D. | 能與Na2CO3溶液反應,也能與NaHCO3溶液反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
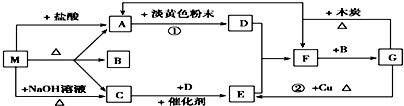
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com