
分析 (1)根據蓋斯定律計算書寫熱化學方程式;
(2)根據平衡體系中各組分的體積分數均為$\frac{1}{4}$,利用三段式計算出平衡時各組分的含量,計算平衡常數和轉化率;
(3)①依據轉化率曲線分析判斷;
②圖象分析速率隨溫度變化的趨勢分析回答;
(4)①鹽對應的酸越弱,對應鹽水解程度越大,堿性越強,pH值越大;
②向0.1mol/L的HCOOH溶液中加水或加入少量HCOONa晶體時,HCOO-離子濃度變大,電離解平衡逆向移動.
解答 解:(1)根據(Ⅰ)CH4(g)+CO2(g)?2CO(g)+2H2(g)△H1=+247.3kJ•mol-1
(Ⅱ)CO(g)+2H2(g)?CH3OH(g)△H2=-90.1kJ•mol-1
(Ⅲ)2CO(g)+O2(g)?2CO2(g)△H3=-566.0kJ•mol-1
由(Ⅰ)×2+(Ⅱ)×2+(Ⅲ)得2CH4(g)+O2(g)?2CH3OH(g)△H,故△H=2△H1+2△H2+△H3=(+247.3kJ•mol-1)×2+(-90.1kJ•mol-1)×2+(-566.0kJ•mol-1)=-251.6kJ•mol-1,所以用CH4和O2直接制備甲醇蒸氣的熱化學方程式為2CH4(g)+O2(g)?2CH3OH(g)△H=-251.6kJ•mol-1,
故答案為:2CH4(g)+O2(g)?2CH3OH(g)△H=-251.6kJ•mol-1;
(2)CH4(g)+CO2(g)?2CO(g)+2H2(g)
起始(mol) 6 6 0 0
變化(mol) x x 2x 2x
平衡(mol)6-x 6-x 2x 2x
平衡體系中各組分的體積分數均為$\frac{1}{4}$,所以6-x=2x,解得x=2,
則此溫度下該反應的平衡常數X=$\frac{{c}^{2}(CO)•{c}^{2}({H}_{2})}{c(C{H}_{4})•c(C{O}_{2})}$=$\frac{{1}^{2}×{1}^{2}}{1×1}$=1,
CH4的轉化率為$\frac{2}{6}$×100%=33.3%,
故答案為:1;33.3%;
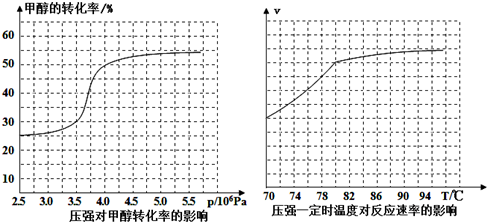
(3)①從反應壓強對甲醇轉化率的影響“效率“看,圖象中轉化率變化最大的是4.0×106Pa,故答案為:4.0×106Pa;
②依據圖象分析溫度在高于80°C對反應速率影響不大,反應是放熱反應,溫度過高,平衡逆向進行,不利于轉化率增大,
故答案為:高于80℃時,溫度對反應速率影響較小,且反應放熱,升高溫度時平衡逆向移動,轉化率降低;
(4)①鹽對應的酸越弱,對應鹽水解程度越大,堿性越強,pH值越大,已知25℃時0.1mol/L的HCOOH溶液和0.1mol/L的CH3COOH溶液的pH分別為2.3和2.9,所以HCOOH的酸性強于CH3COOH,所以pH由大到小順序為②>①>③,故答案為:②>①>③;
②向0.1mol/L的HCOOH溶液中加水或加入少量HCOONa晶體時,HCOO-離子濃度變大,電離平衡逆向移動,
a.電離平衡逆向移動,溶液的pH增大,故正確;
b.電離平衡逆向移動,HCOOH的電離程度減小,故錯誤;
c.離子濃度變大,溶液的導電能力增強,故錯誤;
d.電離平衡逆向移動,氫離子濃度減小,溶液中c(OH-)增大,故錯誤;
故選a.
點評 本題考查了蓋斯定律的應用、熱化學方程式的計算書寫、化學平衡的計算、圖象分析判斷以及弱電解質電離,側重考查外界條件改變對電離平衡的影響,注意掌握基礎知識的掌握,題目難度中等.


 探究與鞏固河南科學技術出版社系列答案
探究與鞏固河南科學技術出版社系列答案科目:高中化學 來源: 題型:解答題
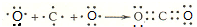 .
.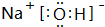 ,其中存在的化學鍵有離子鍵、共價鍵.
,其中存在的化學鍵有離子鍵、共價鍵.查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | Ba(OH)2溶液與稀H2SO4反應:Ba2++SO42-+H++OH-═BaSO4↓+H2O | |
| B. | 往FeCl3溶液中加入Cu粉:Fe3++Cu═Fe2++Cu2+ | |
| C. | Al(OH)3沉淀中滴加鹽酸 Al(OH)3+3H+═Al3++3H2O | |
| D. | FeCl2溶液中通入Cl2:2Fe2++Cl2═2Fe3++2Cl- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CH30H | B. | CH3COCH3 | C. | CH3COOH | D. | CH3COOCH3 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 僅②③⑥ | B. | 僅④⑤⑥ | C. | 僅①④ | D. | 僅②⑥ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com