
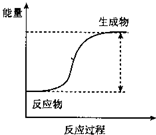
 (1)反應的分類研究:從能量變化角度分,將反應分為放熱反應和吸熱反應.下列反應中能量變化符合如圖所示的是
(1)反應的分類研究:從能量變化角度分,將反應分為放熱反應和吸熱反應.下列反應中能量變化符合如圖所示的是| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |


 永乾教育寒假作業快樂假期延邊人民出版社系列答案
永乾教育寒假作業快樂假期延邊人民出版社系列答案科目:高中化學 來源: 題型:
| 13 |
| 2 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、若混合后溶液pH=7,則c(NH4+)═c(Cl-) |
| B、若b=2a,則c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| C、若a=2b,則(NH4+)>c(Cl-)>c(OH-)>c(H+) |
| D、若混合后溶液滿足c(H+)═c(OH-)+c(NH3?H2O),則可推出a=b |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、①③ | B、②④ | C、①④ | D、②③ |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、HCl的水溶液顯酸性,則NH3的水溶液也顯酸性 |
| B、常溫下鋁投入濃硫酸、濃硝酸中都沒有氣泡產生,則常溫下鋁投入濃鹽酸中也沒有氣泡產生 |
| C、常溫下鋁易與氧氣反應,則常溫下鎂也易與氧氣反應 |
| D、氧化鎂不能溶解在氫氧化鈉溶液中,則氧化鋁也不能溶解在氫氧化鈉溶液中 |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com