
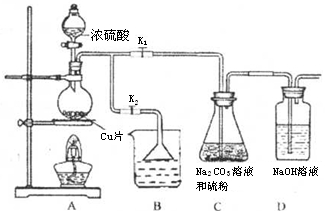
(9分)硫代硫酸鈉又名“大蘇打”,溶液具有弱堿性和較強的還原性,是棉織物漂白后的脫氯劑,定量分析中的還原劑。硫代硫酸鈉(Na2S2O3)可由亞硫酸鈉和硫粉通過化合反應制得,裝置如圖所示
已知:Na2S2O3在酸性溶液中不能穩定存在。
(1)某研究小組設計了制備Na2S2O3·5H2O裝置和部分操作步驟如下:
步驟1:如圖連接好裝置后, ,將D中導管末端浸入水中,微熱燒瓶觀察氣泡和水柱檢查裝置A、C、D氣密性。
步驟2:加入藥品,打開K1、關閉K2,向圓底燒瓶中加入足量濃硫酸,加熱。裝置B中的藥品可選用下列物質中的。
A.NaOH溶液 B.濃H2SO4 C.酸性KMnO4溶液 D.飽和NaHSO3溶液
步驟3:C中混合液被氣流攪動,反應一段時間后,硫粉的量逐漸減少,當C中溶液的pH 接近7時,打開K2 ,關閉K1即停止C中的反應,停止加熱。“當C中溶液的pH接近7時即停止C中的反應”的原因是______________________(用離子方程式表示)。
步驟4:過濾C中的混合液,將濾液經過加熱濃縮,趁熱過濾,再將濾液冷卻結晶、過濾、洗滌、烘干,得到產品。
(2)Na2S2O3性質的檢驗:向足量的新制氯水中滴加少量Na2S2O3溶液,氯水顏色變淺,檢查反應后溶液中含有硫酸根,寫出該反應的化學方程式_________________。
(3)常用Na2S2O3溶液測定廢水中Ba2+濃度,步驟如下:取廢水25.00mL ,控制適當的酸度加入足量K2Cr2O7溶液,得BaCrO4沉淀;過濾、洗滌后,用適量稀鹽酸溶解,此時CrO42-全部轉化為Cr2O72-;再加過量KI溶液,充分反應后得混合溶液V mL,將其分成4等份,加入淀粉溶液作指示劑,用0.0010 mol·L-1 的Na2S2O3溶液進行滴定,相關數據記錄如下表所示:
編號 | 1 | 2 | 3 | 4 |
消耗Na2S2O3標準溶液的體積/mL | 18.02 | 17.98 | 18.00 | 20.03 |
部分反應離子方程式為:
①Cr2O72- + 6I- + 14H+ = 2Cr3+ + 3I2 + 7H2O ;②I2 + 2S2O32- = 2I- + S4O64-。
則判斷達到滴定終點的現象是__________________。
廢水中Ba2+的物質的量濃度為__________________。
科目:高中化學 來源:2015-2016學年甘肅省高一上段中考試化學試卷(解析版) 題型:選擇題
某溶液中含有較大量的Cl﹣、CO32-、OH﹣等三種陰離子,如果只取一次該溶液就能夠分別將三種陰離子依次檢驗出來,下列實驗操作順序正確的是
①滴加Mg(NO3)2溶液 ②過濾 ③滴加AgNO3溶液 ④滴加Ba(NO3)2溶液
A.①②④②③ B.④②①②③
B.①②③②④ D.④②③②①
查看答案和解析>>
科目:高中化學 來源:2015-2016學年青海省高二上9月質檢化學試卷(解析版) 題型:選擇題
在同溫同壓下,下列各組熱化學方程式中Q2> Q1的是
A.H2(g)+Cl2(g)=2HCl(g) △H= -Q1;
1/2H2(g)+1/2Cl2(g)=HCl(g) △H= -Q2
B.C(s)+1/2O2(g)=CO (g) △H= -Q1;
C(s)+ O2(g)=CO2(g) △H= -Q2
C.2H2(g)+O2(g)=2H2O(l) △H= -Q1;
2H2(g)+O2(g)=2H2O(g) △H= -Q2
D.S(g)+O2(g)=SO2(g) △H= -Q1;
S(s)+O2(g)=SO2(g) △H= -Q2
查看答案和解析>>
科目:高中化學 來源:2015-2016學年重慶一中高一上學期10月月考化學試卷(解析版) 題型:選擇題
苯作萃取劑,并用分液漏斗萃取溴水中的溴單質的實驗,下列說法正確的是
A.不能使用酒精作為萃取劑,因為溴單質在酒精中的溶解度比在水中的小
B.靜置分層后有色層在下層,水層幾乎無色
C.分液漏斗使用前應當用蒸餾水檢驗是否漏液
D.振蕩、靜置分層后,依次用兩個不同的燒杯從下口分別接取上下兩層液體
查看答案和解析>>
科目:高中化學 來源:2016屆黑龍江雙鴨山第一中學高三上學期期中測試化學試卷(解析版) 題型:填空題
(14分)元素周期表的用途廣泛。
(1)用“>”或“<”填空:
離子半徑 | 非金屬性 | 酸性 | 沸點 |
K+_____S2- | N____O | 硫酸_____高氯酸 | HF____HCl |
(2)能作為氯、溴、碘元素非金屬性(原子得電子能力)遞變規律的判斷依據是 (填序號)。
a.Cl2、Br2、I2的熔點 b. Cl2、Br2、I2的氧化性
c.HCl、HBr、HI的熱穩定性 d. HCl、HBr、HI的酸性
(3)工業上,通過如下轉化可制得KClO3晶體:
NaCl溶液 NaClO3溶液
NaClO3溶液 KClO3晶體
KClO3晶體
①完成I中反應的總化學方程式:□NaCl+□H2O=□NaClO3+□ 。
②II中轉化的基本反應類型是 ,該反應過程能析出KClO3晶體而無其它晶體析出的原因是 。
(4)一定條件,在水溶液中1 mol Cl-、ClOx-(x=1,2,3,4)的能量(KJ)相對大小如右圖所示。
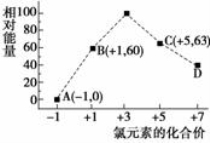
①D是 (填離子符號)。
②B→A+C反應的熱化學方程式為 (用離子符號表示)
查看答案和解析>>
科目:高中化學 來源:2016屆廣東省揭陽市高三上學期第二次月考化學試卷(解析版) 題型:選擇題
如圖進行實驗,試管中現象對應的離子方程式不正確的是
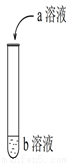
選項 | a | b | 試管中現象 | 離子方程式 |
A | 硫酸 | KI淀粉 | 在空氣中放置一段時間后溶液呈藍色 | 4H++ 4I- + O2=2I2 + 2H2O |
B | 稀鹽酸 | Na2CO3 | 開始時無氣泡,后來有氣泡 | CO HCO |
C | 稀鹽酸 | Na2SiO3 | 產生白色膠狀物 | 2H++ SiO |
D | 硫酸 | 滴有酚酞Ba(OH)2 | 有白色沉淀生成,溶液由紅色變為無色 | Ba2+ + OH- + H+ + SO BaSO4↓ + H2O |
查看答案和解析>>
科目:高中化學 來源:2016屆河北省高三上學期期中測試化學試卷(解析版) 題型:選擇題
一定條件下,中學化學常見物質甲、乙之間存在如下轉化關系,Z是
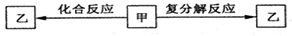
A.HCl B.FeCl2 C.KOH D.NaHCO3
查看答案和解析>>
科目:高中化學 來源:2016屆貴州省遵義市高三上學期第一次聯考化學試卷(解析版) 題型:推斷題
【有機化學基礎】(1 5分)化合物A(C12H16O2)經堿性水解、酸化后得到B和C(C8H8O2)。C的核磁共振氫譜表明含有苯環且苯環上有2種化學環境氫。B經過下列反應后得到G,G由碳、氫、氧三種元素組成,相對分子質量為172,元素分析表明,含碳55.8%,含氫7.0%,核磁共振氫譜顯示只有一個峰。
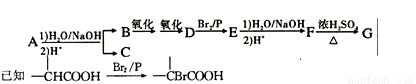
請回答下列問題:
(1)寫出G的分子式: 。
(2)寫出A的結構簡式:____ 。
(3)寫出F—→G反應的化學方程式:____ ,該反應屬于 (填反應類型)。
(4)寫出滿足下列條件的C的所有同分異構體的結構簡式: 。
①是苯的對位二取代化合物;
②能與FeCl3溶液發生顯色反應;
③不考慮烯醇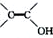 結構。
結構。
(5)在G的粗產物中,經檢測含有聚合物雜質。寫出聚合物雜質可能的結構簡式
(只要寫出1種)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com