
分析 根據阿伏加德羅定律定律比較分子數、物質的量之比,根據分子組成判斷原子數目的多少,根據m=n•M計算質量,根據同溫同壓下,氣體的密度之比等于相對分子質量之比比較密度.
解答 解:根據阿伏加德羅定律定律,相同條件下,相同體積的任何氣體都含有相同的數目的粒子,
則:同溫同壓下,同體積的甲烷(CH4)和二氧化碳分子數之比為1:1;
根據N=n•NA可知:物質的量之比為1:1;
1個甲烷分子中含有5個原子,1個二氧化碳分子中含有3個原子,則原子總數之比為5:3;
根據m=n•M可知,物質的量相同時,質量之比等于相對分子質量之比,則質量之比為16:44=4:11;
根據同溫同壓下,氣體的密度之比等于相對分子質量之比,則密度之比為4:11.
故答案為:1:1;5:3;4:11;4:11.
點評 本題考查物質的量的有關計算以及阿伏加德羅定律及推論的應用,題目難度不大,注意物質的量與質量、體積、微粒數目之間的計算公式的運用.


 學練快車道口算心算速算天天練系列答案
學練快車道口算心算速算天天練系列答案科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na2O2用作呼吸面具的供氧劑 | B. | 實驗室制二氧化碳 | ||
| C. | 工業上利用合成氨實現人工固氮 | D. | 工業上電解熔融狀態Al2O3制備Al |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 微粒組 | 所加試劑 | 離子方程式 |
| A | NH4+、Fe2+、SO42- | 少量Ba(OH)2溶液 | 2NH4++SO42-+Ba2++2OH-═BaSO4↓+2NH3•H2O |
| B | Mg2+、Cl-、HCO3- | 過量NaOH溶液 | Mg2++2HCO3-+4OH-═Mg(OH)2↓+2CO32-+2H2O |
| C | Fe2+、NO3-、HSO3- | NaHSO4溶液 | HSO3-+H+═SO2↑+H2O |
| D | K+、CO32-、NH3•H2O | 通入少量CO2 | CO32-+CO2+2H2O═2HCO3- |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
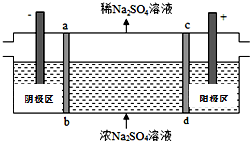 三室式電滲析法處理含Na2SO4廢水的原理如圖所示,采用惰性電極,ab、cd均為離子交換膜,在直流電場的作用下,兩膜中間的Na+和SO42-可通過離子交換膜,而兩端隔室中離子被阻擋不能進入中間隔室.下列敘述正確的是( )
三室式電滲析法處理含Na2SO4廢水的原理如圖所示,采用惰性電極,ab、cd均為離子交換膜,在直流電場的作用下,兩膜中間的Na+和SO42-可通過離子交換膜,而兩端隔室中離子被阻擋不能進入中間隔室.下列敘述正確的是( )| A. | 通電后中間隔室的SO42-離子向正極遷移,正極區溶液堿性增強 | |
| B. | 該法在處理含Na2SO4廢水時可以得到NaOH和H2SO4產品 | |
| C. | 陰極區溶液pH降低,陽極區溶液pH升高 | |
| D. | 當電路中通過1mol電子的電量時,會有0.5mol的O2生成 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
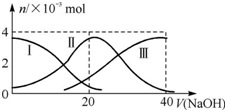 常溫下,向20mL 0.2mol•L-1 H2A溶液中滴加0.2mol•L-1 NaOH溶液.有關微粒的物質的量變化如圖所示.根據圖示判斷下列說法正確的是( )
常溫下,向20mL 0.2mol•L-1 H2A溶液中滴加0.2mol•L-1 NaOH溶液.有關微粒的物質的量變化如圖所示.根據圖示判斷下列說法正確的是( )| A. | 當V(NaOH)=20 mL時,溶液中離子濃度大小關系:c(Na+)>c(HA-)>c(A2-)>c(H+)>c(OH-) | |
| B. | 等濃度的NaOH溶液與H2A溶液按2:1混合后,其溶液中水的電離程度比純水小 | |
| C. | NaHA溶液中:c(OH-)+c(A2-)=c(H+)+c(H2A) | |
| D. | 向上述加入20 mL NaOH溶液后所得溶液中再加入水的過程中,pH可能減小 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com