
 某同學在研究前18號元素時發現,可以將它們排成如圖所示的“蝸牛”形狀,圖中每個“•”代表一種元素,其中O點代表氫元素.下列說法中錯誤的是( )
某同學在研究前18號元素時發現,可以將它們排成如圖所示的“蝸牛”形狀,圖中每個“•”代表一種元素,其中O點代表氫元素.下列說法中錯誤的是( )| A. | 離O點越遠的元素原子半徑越大 | |
| B. | 虛線相連的元素處于同一族 | |
| C. | B元素是圖中金屬性最強的元素 | |
| D. | A、B組成的化合物中可能含有共價鍵 |
分析 0點代表氫元素,按照原子序數由小到大由里往外延伸,由圖可知,O、B連線的三元素為第ⅠA族,A為O元素,B為Na元素,C為Al元素,根據元素的種類可知虛線相連的元素處于同一族,結合對應元素的性質解答該題.
解答 解:A.離O點越遠的元素原子的核電荷數增大,若電子層相同,半徑越小,故A錯誤;
B.由原子序數可知,虛線相連的元素處于同一族,故B正確;
C.B為Na元素,是圖中金屬性最強的元素,故C正確;
D.鈉與氧元素可以形成過氧化鈉,過氧根離子中氧原子之間為非極性鍵,故D正確;
故選A.
點評 本題主要考查元素周期表、元素周期律、化學鍵等,難度不大,看懂圖象推斷元素是解題的關鍵,注意對元素周期表的整體把握.


科目:高中化學 來源: 題型:選擇題
| A. | Z的離子半徑比W的離子半徑小 | |
| B. | 第一電離能:X<Y | |
| C. | Y的氫化物的沸點比Z的氫化物沸點高 | |
| D. | 室溫時,WXY3在純水存在沉淀溶解平衡 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用容量瓶配制溶液時,必須先用該溶液潤洗 | |
| B. | 在蒸餾實驗時常加入碎瓷片以防止暴沸 | |
| C. | 可用堿式滴定管量取20.00mLKMnO4溶液 | |
| D. | 分液操作中,待下層液體流出后,再將上層液體從分液漏斗下口放出 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
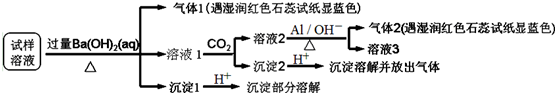
| A. | 試樣中肯定存在NH4+、SO42-和NO3-,可能有Mg2+ | |
| B. | 試樣中不一定存在Na+、Cl-、HCO3- | |
| C. | 沉淀2中可能含碳酸鋇、碳酸鎂和氫氧化鋁 | |
| D. | 該霧霾中可能存在NaNO3、NH4HCO3和MgSO4 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 加入溶液 | ①適量鉍酸鈉溶液 | ②過量的雙氧水 | ③適量KI淀粉溶液 |
| 實驗現象 | 溶液呈紫紅色 | 紫紅色消失,產生氣泡 | 溶液變成藍色 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
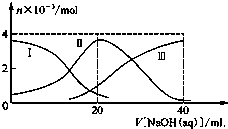 常溫下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有關微粒的物質的量變化如圖所示(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-),根據圖示判斷,下列說法正確的是( )
常溫下,向20mL 0.2mol/L H2A溶液中滴加0.2mol/L NaOH溶液.有關微粒的物質的量變化如圖所示(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-),根據圖示判斷,下列說法正確的是( )| A. | 當V[NaOH(aq)]=20 mL時,溶液中離子濃度大小關系:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) | |
| B. | 等體積等濃度的NaOH溶液與H2A溶液混合后,其溶液中水的電離程度比純水大 | |
| C. | H2A第一步電離的方程式為H2A→HA-+H+ | |
| D. | 向NaHA溶液加入水稀釋的過程中,pH可能增大也可能減少 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 以金屬銀為陽極電解飽和NaCl溶液:2Cl-+2H2O=H2↑+Cl2↑+2OH- | |
| B. | FeBr2溶液中通入足量的氯氣:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- | |
| C. | 硫酸亞鐵溶液中加入用硫酸酸化的雙氧水Fe2++2H++H2O2=Fe3++2H2O | |
| D. | 在通入過量SO2后的NaOH溶液中加足量的溴水(不考慮SO2的溶解):HSO3-+Br2+H2O=3H++2Br-+SO42- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 利用二氧化碳等原料合成的聚碳酸酯類可降解塑料替代聚乙烯塑料,可減少“白色污染” | |
| B. | 硅晶體的導電性介于導體與絕緣體之間,是一種重要的半導體材料,廣泛應用于制造集成電路、光導纖維、太陽能電池板等 | |
| C. | pH計不能用于酸堿中和滴定終點的判斷 | |
| D. | 2013年11月22日,中科院國家納米科學中心宣布,該中心科研人員在國際上首次“拍”到氫鍵的“照片”,實現了氫鍵的實空間成像,為“氫鍵的本質”這一化學界爭論了80多年的問題提供了直觀證據.水分子間的氫鍵是一個水分子中的氫原子與另一個水分子中的氧原子間形成的化學鍵 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 銨鹽是一種重要的水體污染物.某課題組利用電解法,在含Cl-的水樣中,探究將NH4+轉化為N2而脫氮的影響因素和反應機理.
銨鹽是一種重要的水體污染物.某課題組利用電解法,在含Cl-的水樣中,探究將NH4+轉化為N2而脫氮的影響因素和反應機理.| 實驗方案 | 預期實驗結果和結論 |
| 配制一定pH、NH4+和Cl-濃度的溶液,用最佳電流強度,電解樣品90min后,采用電子自旋共振法檢測樣品中•OH |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com