
| A. | 銅是還原劑,發生了氧化反應 | |
| B. | 每生成64 g SO2,轉移電子的物質的量是2 mol | |
| C. | 每消耗1 mol Cu,起氧化劑作用的硫酸消耗2 mol | |
| D. | 在此反應中,濃硫酸表現出酸性和氧化性 |
分析 發生Cu+2H2SO4(濃)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+H2O,利用化合價的變化分析氧化劑、還原劑、消耗的酸及轉移的電子數,以此來解答.
解答 解:A.反應中Cu元素的化合價由0升高到+2價,作還原劑,發生氧化反應,故A正確;
B.由Cu+2H2SO4(濃)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+H2O可知,每生成1molSO2,即64 g SO2,轉移電子的物質的量為1mol×(6-4)=2mol,故B正確;
C.由Cu+2H2SO4(濃)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+H2O可知,每消耗1molCu,起氧化劑作用的硫酸消耗1mol,故C錯誤;
D.該反應有硫酸銅生成,體現酸性,生成二氧化硫體現其氧化性,故D正確;
故選C.
點評 本題考查銅與濃硫酸的反應及氧化還原反應計算,為高頻考點,把握發生的化學反應及利用化合價分析氧化還原反應為解答的關鍵,側重分析與應用能力的考查,題目難度不大.


 輕松暑假總復習系列答案
輕松暑假總復習系列答案科目:高中化學 來源: 題型:選擇題
| A. | -CHO的電子式: | B. | 丙烷分子的比例模型為: | ||
| C. | 順-1,2-二溴乙烯結構式為: | D. | 1,4-二甲苯的結構簡式為: |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①③④ | B. | ③⑦ | C. | ③⑤ | D. | ⑥ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 中和反應是吸熱反應 | |
| B. | 燃燒屬于放熱反應 | |
| C. | 斷裂化學鍵要放出能量 | |
| D. | 反應物總能量一定等于生成物總能量 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
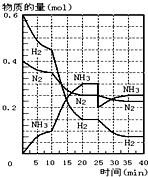 (1)在一定條件下,將H2和N2置于一容積為2L的密閉容器中發生反應.反應過程中H2、N2和NH3的物質的量變化如圖:
(1)在一定條件下,將H2和N2置于一容積為2L的密閉容器中發生反應.反應過程中H2、N2和NH3的物質的量變化如圖:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
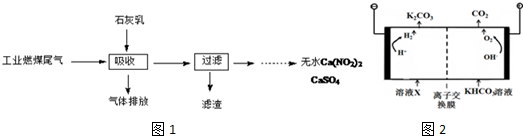
 H2SO3、2H2SO3+O2$\frac{\underline{\;催化劑\;}}{\;}$2H2SO4.
H2SO3、2H2SO3+O2$\frac{\underline{\;催化劑\;}}{\;}$2H2SO4.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0 | B. | 175 | C. | 57 | D. | 118 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 同主族元素形成的單質熔沸點自上而下逐漸升高 | |
| B. | 核外電子排布相同的微粒化學性質不一定相同 | |
| C. | 第三周期中,除稀有氣體元素外原子半徑最大的是氯 | |
| D. | 同主族元素氫化物的穩定性越強其沸點就越高 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com