
| A. | H+ | B. | SO42- | C. | OH- | D. | Na+ |
科目:高中化學 來源: 題型:選擇題
| A. | 某藍色溶液中加NaOH溶液,生成藍色沉淀,說明原溶液中有Cu2+ | |
| B. | 某溶液中加BaCl2溶液,生成白色沉淀,繼續滴加稀硝酸沉淀不溶解,說明原溶液中有SO42- | |
| C. | 某溶液中加硝酸銀溶液,生成白色沉淀,繼續滴加稀硝酸有部分沉淀不溶解,說明原溶液中一定有Cl- | |
| D. | 某溶液中加稀硫酸溶液生成無色無味氣體,該氣體能使澄清石灰水變渾濁,說明原溶液中一定含有CO32- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①③⑤⑧ | B. | ②③④⑤⑥⑦ | C. | ③⑤⑧ | D. | ①②③④⑤⑥⑦⑧ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 銅合金是人類使用最早的金屬材料.銅在化合物中的常見化合價有+l、+2 等,故能形成多種銅的化合物.
銅合金是人類使用最早的金屬材料.銅在化合物中的常見化合價有+l、+2 等,故能形成多種銅的化合物. 查看答案和解析>>
科目:高中化學 來源: 題型:填空題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 若有9.8gH2SO4參加反應,則轉移電子的物質的量為1mol | |
| B. | 該反應的化學方程式為:5PbO2+2MnSO4+2H2SO4═Pb(MnO4)2+4PbSO4+2H2O | |
| C. | Pb(MnO4)2既是氧化產物又是還原產物 | |
| D. | X是MnSO4 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
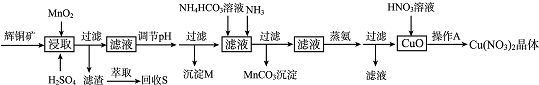
| 離子 | 開始沉淀的pH | 完全沉淀的pH |
| Fe3+ | 1.1 | 3.2 |
| Mn2+ | 8.3 | 9.8 |
| Cu2+ | 4.4 | 6.4 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com