
常溫下,取0.3 mol/L HY溶液與0.3 mol/L NaOH溶液等體積混合(不計混合后溶液體積變化),測得混合溶液的pH=9,則下列說法(或關系式)正確的是
A.混合溶液中由水電離出來的c(OH-)=1×10-9 mol/L
B.混合溶液中離子濃度大小次序為:c(Y-)>c(Na+)>c(OH-)>c(H+)
C.c(OH-)-c(HY)=c(H+)=1×10-9 mol/L
D.c(Na+)=c(Y-)+c(HY)="0.3" mol/L
C
【解析】
試題分析:等體積混合后,溶液的溶質應該為NaY,濃度應該為0.15mol/L,但是最后溶液顯堿性,說明發生了水解。A選項錯誤,由pH值計算得到氫離子的濃度為1×10-9 mol/L,則氫氧根離子的濃度應該為1×10-5 mol/L。B選項由于NaY發生水解,則c(Y-)<c(Na+),錯誤。C選項正確,此等式為質子守恒。D選項最后溶液體積為原來的兩倍,鈉離子的濃度應該是原來的一半,則為0.15mol/L。
考點:鹽類的水解
點評:本題涉及到了一個難點知識鹽類的水解,學生在做題時經常會遇到的問題有離子濃度大小的判斷,鹽類水解中的三個守恒關系的判定,這些需要學生多加練習,熟能生巧。


科目:高中化學 來源: 題型:
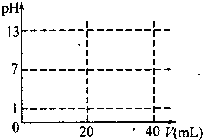 (2012?成都模擬)溶液中的化學反應大多是離子反應.根據要求回答下列問題.
(2012?成都模擬)溶液中的化學反應大多是離子反應.根據要求回答下列問題.查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解

| ||
| ||
查看答案和解析>>
科目:高中化學 來源: 題型:
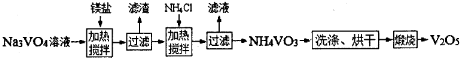
查看答案和解析>>
科目:高中化學 來源: 題型:
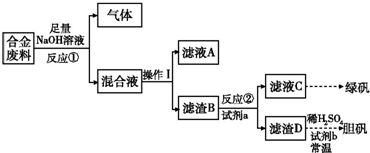
| 實驗編號 | 1 | 2 | 3 | 4 |
| 稀HNO3體積(mL) | 100 | 200 | 300 | 400 |
| 剩余金屬質量(g) | 9.0 | 4.8 | 0 | 0 |
| NO體積(L) | 1.12 | 2.24 | 3.36 | V |
查看答案和解析>>
科目:高中化學 來源: 題型:
www.ks5u.co m
A、B、C是三種常見短周期元素的單質。常溫下D為無色液體,E是一種常見的溫室氣體。其轉化關系如圖17 (反應條件和部分產物略去)。試回答:
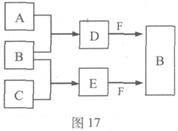
(1)E的電子式是 。
(2)單質X和B或D均能反應生成黑色固體Y,Y的化學式是 。
(3)物質Z常用于對空氣進行殺菌、凈化和水果保鮮等。Z和B的組成元素相同,Z分子中各原子最外層電子數之和為18。Z和酸性碘化鉀溶液反應生成B和碘單質,反應的離子方程式是 。
(4)取0.3 mol F與足量D充分混合后,所得溶液中再通入0.2 mol E充分反應,最后得到的水溶液中各種離子的濃度由大到小的順序是(不考慮H+) 。
(5)E的大量排放會引發很多環境問題。有科學家提出,用E和H2合成CH3OH和H2O,對E進行綜合利用。25℃,101 kPa時,該反應的熱化學方程式是 。
(已知甲醇的燃燒熱![]() ,氫氣的燃燒熱
,氫氣的燃燒熱![]() )
)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com