隨著材料科學的發展,金屬釩及其化合物得到了越來越廣泛的應用.
(1)釩主要用來制造釩鋼.釩鋼具有很高的耐磨損性和抗撞擊性,原因是
(填序號)
A.釩在常溫下,化學活潑性較弱
B.釩鋼表面形成了致密且堅固的氧化膜
C.釩鋼結構緊密,具有較高的韌性、彈性和強度
(2)在溫度較低時,溶液中釩酸鹽會轉化為焦釩酸鹽:
2VO
43-+H
2O?V
2O
74-+2OH
-①
在溫度較高時,焦釩酸鹽又轉化為偏釩酸鹽:
V
2O
74-+H
2O?2VO
3-+2OH
-②
反應②平衡常數的表達式K=
;
(3)已知某溫度下:4V(s)+5O
2(g)=2V
2O
5(s)△H=-1551kJ?mol
-14V(s)+3O
2(g)=2V
2O
3(s)△H=-1219kJ?mol
-12H
2(g)+O
2(g)=2H
2O(l)△H=-571.6kJ?mol
-1寫出H
2還原V
2O
5得到V
2O
3的熱化學方程式:
;
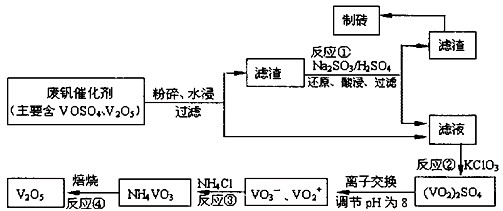
(4)用釩酸鈉(Na
3VO
4)溶液(含PO
43-、SiO
32-等雜質離子)制備高純V
2O
5流程如下:
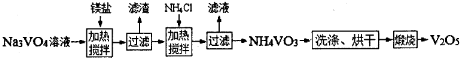
①加入鎂鹽,加熱攪拌,其中加熱的作用是
;
②在25℃時,K
sp[Mg
3(PO
4)
2]=1.0×10
-26,若凈化后溶液中的Mg
2+的平衡濃度為 1.0×10
-4 mol?L
-1,則溶液中c(P0
43-)=
;
③加入NH
4Cl,加熱攪拌,該步驟反應的離子方程式為
;
④為測定產品純度,稱取產品mg,溶解后定容在100mL容量瓶中,每次取5.00mL溶液于錐形瓶中,加入一定量的稀鹽酸和KI溶液,用a mol?L
-1Na
2S
2O
3標準溶 液滴定,發生的反應為:
V
2O
5+6HCl+2KI=2VOCl
2+2KCl+I
2+3H
2O
I
2+2Na
2S
2O
3=Na
2S
4O
6+2NaI
若三次滴定消耗標準溶液的平均體積為bmL,則該產品的純度為
(用含m、a、b的代數式表示).





 其中a、c二步的化學方程式可表示為
其中a、c二步的化學方程式可表示為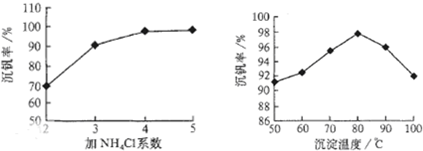
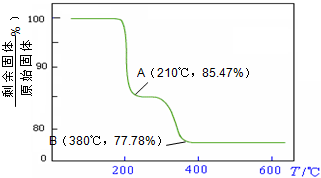 則NH4VO3在分解過程中
則NH4VO3在分解過程中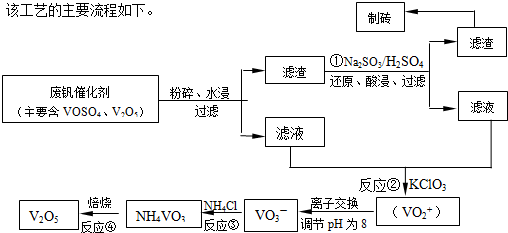
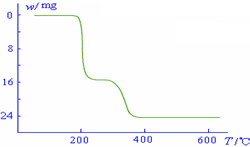 化的曲線如右圖所示.則NH4VO3在分解過程中
化的曲線如右圖所示.則NH4VO3在分解過程中