
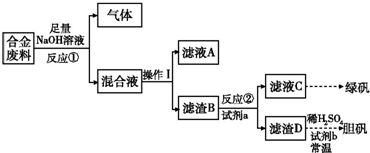
| 實驗編號 | 1 | 2 | 3 | 4 |
| 稀HNO3體積(mL) | 100 | 200 | 300 | 400 |
| 剩余金屬質量(g) | 9.0 | 4.8 | 0 | 0 |
| NO體積(L) | 1.12 | 2.24 | 3.36 | V |


 第1卷單元月考期中期末系列答案
第1卷單元月考期中期末系列答案科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
2- 7 |
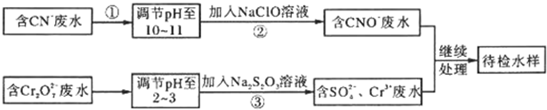
| S2O | 2- 3 |
2- 7 |
| SO | 2- 4 |
2- 7 |
查看答案和解析>>
科目:高中化學 來源:素質教育新教案 高中化學·二年級·第二冊(上冊) 題型:043
從某些方面看,氨與水相當;![]() 和H3O+(常寫為H+)相當;
和H3O+(常寫為H+)相當;![]() 和OH-相當,NH2-(有時還包括N3-)和O2-相當
和OH-相當,NH2-(有時還包括N3-)和O2-相當
(1)已知在液氨中能發生如下反應:NH4Cl+KNH2![]() KCl+2NH3,2NH4I+PbNH
KCl+2NH3,2NH4I+PbNH![]() PbI2+3NH3請寫出在水溶液中發生的與上述反應相當的反應方程式.
PbI2+3NH3請寫出在水溶液中發生的與上述反應相當的反應方程式.
(2)寫出并配平下列反應方程(M為金屬)
M+NH3→
MO+NH4Cl→
M(NH2)2![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
已知A—O分別代表一種物質,它們之間的轉化關系如下圖所示(反應條件略)。A、B、H分別是由短周期元素組成的單質。B與冷水緩慢反應,與沸水迅速反應,放出氫氣。D是一種離子化合物,其陰陽離子的個數比為2:3,且能與水反就應得到兩種堿。C為淡黃色固體化合物,O能與G的水溶液反應生成藍色沉淀。請回答下列問題:
⑴組成B單質的元素位于周期表位置________________。化合物C電子式為____________。
⑵J的沸點比硒化氫(H2Se)的熔沸點高,其原因是_________________。
⑶I與H在一定條件下也可直接反應生成L和J, 寫出化學方程式:_______________。
⑷寫出D與水反應的化學方程式:_____________________。
⑸紅棕色污染氣體M的處理具有實際意義。現在常利用反應
M + NH3N2+H2O(方程沒配平)來處理M。當轉移0.4mol電子時,消耗的M在標準狀況下是 L。
查看答案和解析>>
科目:高中化學 來源:2012-2013學年山東省日照市高三第一次模擬考試理綜化學試卷(解析版) 題型:填空題
某工業廢水中含有CN-和Cr2O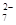 等離子,需經污水處理達標后才能排放,污水處理廠擬用下列流程進行處理:
等離子,需經污水處理達標后才能排放,污水處理廠擬用下列流程進行處理:
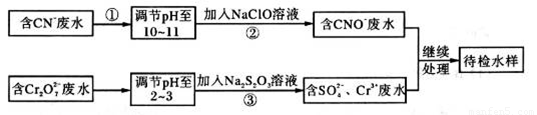
回答下列問題:
(1)步驟②中,CN-被ClO-氧化為CNO-的離子方程式為________________。
(2)步驟③的反應為S2O32-+Cr2O72-+H+ SO42-+Cr3++H2O(未配平),則每消耗0.4mol Cr2O72-轉移__________mol
e-。
SO42-+Cr3++H2O(未配平),則每消耗0.4mol Cr2O72-轉移__________mol
e-。
(3)含Cr3+廢水可以加入熟石灰進一步處理,目的是____________________。
(4)在25℃下,將amol/L的NaCN溶液與0.01mol/L的鹽酸等體積混合,反應后測得溶液pH=7,則a________0.01(填“>”、“<”或“=”);用含a的代數式表示HCN的電離常數Ka=_________________。
(5)取工業廢水水樣于試管中,加入NaOH溶液觀察到有藍色沉淀生成,繼續加至不再產生藍色沉淀為止,再向溶液中加入足量Na2S溶液,藍色沉淀轉化成黑色沉淀。該過程中反應的離子方程是________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com