
分析 n(Na2CO3)=$\frac{10.6g}{106g/mol}$=0.1mol,n(HCl)=0.8mol/L×0.5L=0.4mol,根據Na2CO3+2HCl=2NaCl+H2O+CO2↑知,如果0.1mol碳酸鈉完全反應生成二氧化碳,需要0.2molHCl<0.4mol,則稀鹽酸過量.
(1)根據C原子守恒計算生成二氧化碳體積;
(2)溶液稀釋前后氫離子物質的量不變,根據c=$\frac{n}{V}$計算稀釋后氫離子濃度;
(3)溶液稀釋前后氯離子物質的量不變,據c=$\frac{n}{V}$計算稀釋后Cl-的物質的量濃度.
解答 解:n(Na2CO3)=$\frac{10.6g}{106g/mol}$=0.1mol,n(HCl)=0.8mol/L×0.5L=0.4mol,根據Na2CO3+2HCl=2NaCl+H2O+CO2↑知,如果0.1mol碳酸鈉完全反應生成二氧化碳,需要0.2molHCl<0.4mol,則稀鹽酸過量;
(1)根據C原子守恒得生成V(CO2)=n(CO2)Vm=n(Na2CO3)Vm=0.1mol×22.4L/mol=2.24L,
答:生成二氧化碳的體積(標準狀況)為2.24L;
(2)根據方程式中Na2CO3---2HCl知,0.1mol碳酸鈉完全反應需要0.2molHCl,則剩余n(H+)=0.4mol-0.2mol=0.2mol,溶液稀釋前后氫離子物質的量不變,稀釋后c(H+)=$\frac{n}{V}$=$\frac{0.2mol}{1L}$=0.2mol/L,
答:稀釋后氫離子濃度為0.2mol/L;
(3)反應過程中氯離子不參加反應,且溶液稀釋前后氯離子物質的量不變,根據Cl原子守恒得n(Cl-)=n(HCl)=0.4mol,稀釋后溶液中c(Cl-)=$\frac{n}{V}$=$\frac{0.4mol}{1L}$=0.4mol/L,
答:稀釋后氯離子濃度為0.4mol/L.
點評 本題考查化學方程式有關計算,為高頻考點,側重考查學生分析計算能力,當反應物的物質的量都已知時要進行過量計算,為易錯點.


科目:高中化學 來源: 題型:選擇題
| A. | 溶液的pH變大 | |
| B. | c(Na+)與c(SO42-)的比值不變 | |
| C. | 電解過程中,向陽極附近溶液滴入酚酞,溶液變為紅色 | |
| D. | 陰、陽極產生氣體在相同條件下體積之比為1:2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
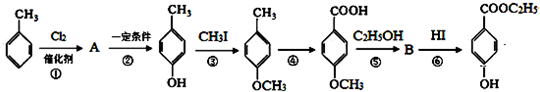
 .
.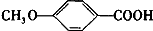 +C2H5OH$?_{△}^{濃硫酸}$
+C2H5OH$?_{△}^{濃硫酸}$ +H2O.
+H2O.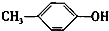 +CH2I→
+CH2I→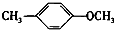 +HI.
+HI.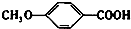 的同分異構體有多種,其中既含有酚羥基又含有酯基的同分異構體共有19種.
的同分異構體有多種,其中既含有酚羥基又含有酯基的同分異構體共有19種.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
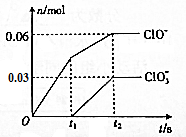 將-定量的Cl2通入一定濃度的苛性鉀溶液中,兩者恰好完全反應(已知反應過程放熱),ClO-和ClO${\;}_{3}^{-}$的物質的量(n)與反應時間(t)的變化關系如圖所示,則t2時刻,n(還原產物):n(氧化產物)為( )
將-定量的Cl2通入一定濃度的苛性鉀溶液中,兩者恰好完全反應(已知反應過程放熱),ClO-和ClO${\;}_{3}^{-}$的物質的量(n)與反應時間(t)的變化關系如圖所示,則t2時刻,n(還原產物):n(氧化產物)為( )| A. | 3:7 | B. | 7:3 | C. | 3:2 | D. | 2:3 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
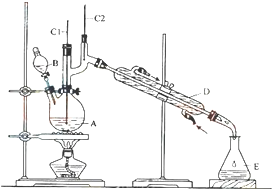 正丁醛是一種化工原料.某實驗小組利用如圖裝置合成正丁醛.發生的反應如下:
正丁醛是一種化工原料.某實驗小組利用如圖裝置合成正丁醛.發生的反應如下:| 沸點/0C | 密度/(g•cm-3) | 水中溶解性 | |
| 正丁醇 | 117.2 | 0.8109 | 微溶 |
| 正丁醛 | 75.7 | 0.8017 | 微溶 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①中水的電離程度最小,③中水的電離程度最大 | |
| B. | 將②、③混合,若pH=7,則消耗溶液的體積②=③ | |
| C. | 將四份溶液稀釋相同的倍數后,溶液的pH:③>④>②>① | |
| D. | 將①、④混合,若有c(CH3COO-)>c(H+),則混合溶液一定呈堿性 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com