
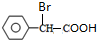 +2NaOH$\stackrel{△}{→}$
+2NaOH$\stackrel{△}{→}$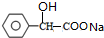 +NaBr+H2O.
+NaBr+H2O.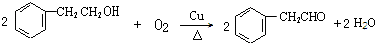 .
.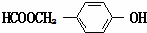 (寫結(jié)構(gòu)簡式).
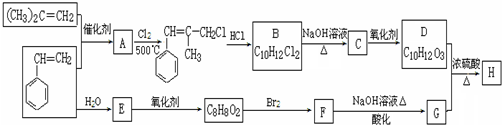
(寫結(jié)構(gòu)簡式). 分析 由A與氯氣在加熱條件下反應生成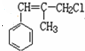 ,可知A的結(jié)構(gòu)簡式為:
,可知A的結(jié)構(gòu)簡式為: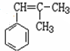 ,故苯乙烯與(CH3)2C=CH2發(fā)生加成反應生成A,
,故苯乙烯與(CH3)2C=CH2發(fā)生加成反應生成A, 與HCl反應生成B,結(jié)合B的分子式可知,應是發(fā)生加成反應,B中核磁共振氫譜圖顯示分子中有6種不同環(huán)境的氫原子,故B為
與HCl反應生成B,結(jié)合B的分子式可知,應是發(fā)生加成反應,B中核磁共振氫譜圖顯示分子中有6種不同環(huán)境的氫原子,故B為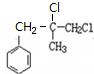 ,順推可知C為
,順推可知C為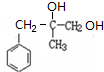 ,D為
,D為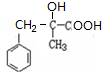 .苯乙烯與水發(fā)生加成反應生成E,E可以氧化生成C8H8O2,說明E中羥基連接的C原子上有2個H原子,故E為
.苯乙烯與水發(fā)生加成反應生成E,E可以氧化生成C8H8O2,說明E中羥基連接的C原子上有2個H原子,故E為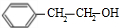 ,C8H8O2為
,C8H8O2為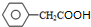 ,
,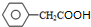 與溴反應生成F,F(xiàn)在氫氧化鈉溶液條件下水解、酸化得到G,且D和G是同系物,故
與溴反應生成F,F(xiàn)在氫氧化鈉溶液條件下水解、酸化得到G,且D和G是同系物,故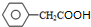 中亞甲基上1個H原子被Br原子取代生成F,F(xiàn)為
中亞甲基上1個H原子被Br原子取代生成F,F(xiàn)為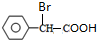 ,G為
,G為 ,D與G生成H,H結(jié)構(gòu)中含有三個六元環(huán),則H為
,D與G生成H,H結(jié)構(gòu)中含有三個六元環(huán),則H為 ,以此解答該題.
,以此解答該題.
解答 解:由A與氯氣在加熱條件下反應生成 ,可知A的結(jié)構(gòu)簡式為:
,可知A的結(jié)構(gòu)簡式為: ,故苯乙烯與(CH3)2C=CH2發(fā)生加成反應生成A,
,故苯乙烯與(CH3)2C=CH2發(fā)生加成反應生成A, 與HCl反應生成B,結(jié)合B的分子式可知,應是發(fā)生加成反應,B中核磁共振氫譜圖顯示分子中有6種不同環(huán)境的氫原子,故B為
與HCl反應生成B,結(jié)合B的分子式可知,應是發(fā)生加成反應,B中核磁共振氫譜圖顯示分子中有6種不同環(huán)境的氫原子,故B為 ,順推可知C為
,順推可知C為 ,D為
,D為 .苯乙烯與水發(fā)生加成反應生成E,E可以氧化生成C8H8O2,說明E中羥基連接的C原子上有2個H原子,故E為
.苯乙烯與水發(fā)生加成反應生成E,E可以氧化生成C8H8O2,說明E中羥基連接的C原子上有2個H原子,故E為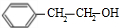 ,C8H8O2為
,C8H8O2為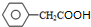 ,
,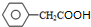 與溴反應生成F,F(xiàn)在氫氧化鈉溶液條件下水解、酸化得到G,且D和G是同系物,故
與溴反應生成F,F(xiàn)在氫氧化鈉溶液條件下水解、酸化得到G,且D和G是同系物,故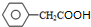 中亞甲基上1個H原子被Br原子取代生成F,F(xiàn)為
中亞甲基上1個H原子被Br原子取代生成F,F(xiàn)為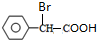 ,G為
,G為 ,D與G生成H,H結(jié)構(gòu)中含有三個六元環(huán),則H為
,D與G生成H,H結(jié)構(gòu)中含有三個六元環(huán),則H為 ,
,
(1)(CH3)2C=CH2系統(tǒng)命名為:2-甲基-1-丙烯,故答案為:2-甲基-1-丙烯;
(2)A與氯氣在加熱條件下發(fā)生取代反應生成 ,
, 與HCl反應發(fā)生加成反應B,故答案為:取代反應、加成反應;
與HCl反應發(fā)生加成反應B,故答案為:取代反應、加成反應;
(3)D為 ,含有的官能團為:羥基、羧基,故答案為:羧基、羥基;
,含有的官能團為:羥基、羧基,故答案為:羧基、羥基;
(4)F與足量氫氧化鈉溶液在加熱條件下反應的化學方程式為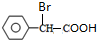 +2NaOH$\stackrel{△}{→}$
+2NaOH$\stackrel{△}{→}$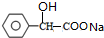 +NaBr+H2O,
+NaBr+H2O,
故答案為: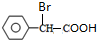 +2NaOH$\stackrel{△}{→}$
+2NaOH$\stackrel{△}{→}$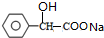 +NaBr+H2O;
+NaBr+H2O;
(5)E在銅催化下與氧氣反應的化學方程式為: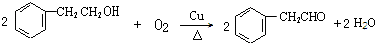 ,
,
故答案為: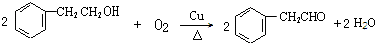 ;
;
(6)G為 ,G的同分異構(gòu)體同時滿足下列條件:①與FeCl3溶液發(fā)生顯色反應,含有酚羥基;②能發(fā)生水解反應,含有酯基;③苯環(huán)上有兩個取代基,為-OH、-OOCCH3或-OH、-CH2OOCH或-OH、-COOCH3,各有鄰、間、對3種位置關系,故符合條件的同分異構(gòu)體共有9種,其中核磁共振氫譜有5個吸收峰同分異構(gòu)體為:
,G的同分異構(gòu)體同時滿足下列條件:①與FeCl3溶液發(fā)生顯色反應,含有酚羥基;②能發(fā)生水解反應,含有酯基;③苯環(huán)上有兩個取代基,為-OH、-OOCCH3或-OH、-CH2OOCH或-OH、-COOCH3,各有鄰、間、對3種位置關系,故符合條件的同分異構(gòu)體共有9種,其中核磁共振氫譜有5個吸收峰同分異構(gòu)體為: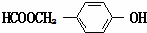 ,故答案為:9;
,故答案為:9;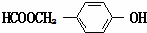 .
.
點評 本題考查有機物的推斷,為高考常見題型,側(cè)重對有機物知識的綜合運用的考查,能較好的考查考生的閱讀、自學能力和思維能力,難度較大,注意充分利用轉(zhuǎn)化關系中物質(zhì)的結(jié)構(gòu)及分子式,結(jié)合正推法與逆推法進行推斷,注意充分利用反應條件,(6)中同分異構(gòu)體數(shù)目判斷與限制條件同分異構(gòu)體書寫為易錯點、難點.


科目:高中化學 來源:2017屆吉林省長春市高三上學期期中考試化學試卷(解析版) 題型:選擇題
某恒溫密閉容器發(fā)生可逆反應Z(?)+W(?) X(g)+Y(?)ΔH,在t1時刻反應達到平衡,在t2時刻縮小容器體積,t3時刻再次達到平衡狀態(tài)后未再改變條件。下列有關說法中正確的是
X(g)+Y(?)ΔH,在t1時刻反應達到平衡,在t2時刻縮小容器體積,t3時刻再次達到平衡狀態(tài)后未再改變條件。下列有關說法中正確的是

A.Z和W在該條件下至少有一個是為氣態(tài)
B.t1~t2時間段與t3時刻后,兩時間段反應體系中氣體的平均摩爾質(zhì)量不可能相等
C.若該反應只在某溫度T0以上自發(fā)進行,則該反應的平衡常數(shù)K隨溫度升高而增大
D.若在該溫度下此反應平衡常數(shù)表達式為K=c(X),則t1~t2時間段與t3時刻后的X濃度不相等
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 對于Si+O2═SiO2,每當新形成2NA個Si-O鍵,需要斷開NA個Si-Si鍵 | |
| B. | 12.0g熔融的NaHSO4中含有的陽離子數(shù)為0.1NA | |
| C. | 次氯酸光照分解產(chǎn)生22.4mL氣體(標準狀況)轉(zhuǎn)移的電子數(shù)為0.002NA | |
| D. | 電解精煉銅時,若陰極析出32g銅,則轉(zhuǎn)移的電子數(shù)為NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 乙醇、乙二醇、丙三醇互為同系物;H2、D2、T2互為同素異形體 | |
| B. | 綠礬、堿石灰、蘇打、干冰分別屬于純凈物、混合物、電解質(zhì)、非電解質(zhì) | |
| C. | 乙烯水化、鐵鋁鈍化、植物油氫化、純堿晶體風化等過程中都包含化學變化 | |
| D. | 蛋白質(zhì)、纖維素、硝化纖維等都是高分子化合物 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 除去NaHCO3溶液中少量的Na2CO3:加入適量稀鹽酸 | |
| B. | 除去FeCl2溶液中少量的FeCl3:加入稍過量鐵粉,過濾 | |
| C. | 除去NH4Cl固體中少量I2:加熱,I2升華除去 | |
| D. | 除去乙烯中的少量SO2:通過酸性KMnO4溶液,洗液 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 .
.查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com