
 氯的氧化物是氯與氧的二元化合物的總稱,也稱為氧化氯.目前Cl2O、ClO2、Cl2O7已能制取.有關數據見下表:
氯的氧化物是氯與氧的二元化合物的總稱,也稱為氧化氯.目前Cl2O、ClO2、Cl2O7已能制取.有關數據見下表:| 化學式 | Cl2O | ClO2 | Cl2O7 |
| 相對分子質量 | 87 | 67.5 | 183 |
| 沸點/℃ | 2 | 9.7 | 81 |
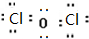 .
.分析 (1)酸酐與對應酸中Cl元素的化合價相同,Cl2O的結構為Cl-O-Cl;
(2)利用氫化物的穩定性、得電子能力等判斷非金屬性;
(3)結構相似的分子,相對分子質量越大,沸點越大;
(4)ClO2和堿溶液反應生成亞氯酸鹽(陰離子是ClO2-)和氯酸鹽,為氧化還原反應,只有Cl元素的化合價變化;
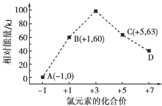
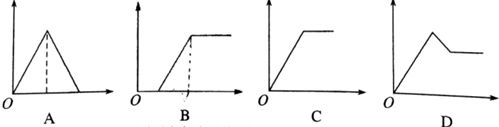
(5)由圖可知,D中Cl元素的化合價為+7價,B→A+C結合轉移電子守恒得該反應方程式為3ClO-=ClO3-+2Cl-,結合圖中能量變化計算反應熱.
解答 解:(1)酸酐與對應酸中Cl元素的化合價相同,則Cl2O是為HClO的酸酐,Cl2O的結構為Cl-O-Cl,其電子式為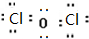 ,
,
故答案為:HClO;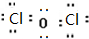 ;
;
(2)a.氧化氯的分子式中O為負價,則非金屬性O大于Cl,故正確;
b.與金屬反應得電子的數目,不能比較非金屬性,故錯誤;
c.氣態氫化物的穩定性強的為水,則非金屬性O大于Cl,故正確;
d.O元素不存在最高價氧化物對應水化物,故錯誤;
故答案為:ac;
(3)上表中相對分子質量是Cl2O7>Cl2O>ClO2,其沸點的變化不是Cl2O7>Cl2O>ClO2的原因是Cl2O7、Cl2O、ClO2結構不相似,不符合分子間作用力對沸點影響的變化規律,故答案為:Cl2O7、Cl2O、ClO2結構不相似,不符合分子間作用力對沸點影響的變化規律;
(4)ClO2和堿溶液反應生成亞氯酸鹽(陰離子是ClO2-)和氯酸鹽,為氧化還原反應,離子反應為2ClO2+2OH-=ClO2-+ClO3-+H2O,Cl元素失去電子被氧化,則氧化產物為ClO3-,
故答案為:2ClO2+2OH-=ClO2-+ClO3-+H2O;ClO3-;
(5)由圖可知,D中Cl元素的化合價為+7價,則D為ClO4-;B→A+C結合轉移電子守恒得該反應方程式為3ClO-=ClO3-+2Cl-,△H=(63kJ/mol+2×0kJ/mol)-3×60kJ/mol=-117kJ/mol,所以該熱化學反應方程式為3ClO-(aq)=ClO3-(aq)+2Cl-(aq)△H=-117kJ/mol,
故答案為:ClO4-;3ClO-(aq)=ClO3-(aq)+2Cl-(aq)△H=-117kJ/mol.
點評 本題考查物質的性質及反應原理,為高頻考點,把握物質的性質、發生的反應、反應熱計算等為解答的關鍵,側重元素化合物知識及反應原理的綜合考查,題目難度不大.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| R | ||
| X | Y | Z |
| A. | 原子半徑大小順序是:Y>X>R | |
| B. | 其氣態氫化物的穩定性順序是:Z>Y>X>R | |
| C. | X、Y、Z中Z的氧化物對應的水化物的酸性最強 | |
| D. | R的氣態氫化物與它的含氧酸之間能發生化學反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | SO2既是氧化產物又是還原產物 | |
| B. | CuFeS2僅作還原劑,硫元素被氧化 | |
| C. | 每生成1 mol Cu2S,同時生成22.4L SO2 | |
| D. | 有0.2 mol硫被氧化時,轉移1.2NA個電子 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 2015年諾貝爾獎獲得者屠呦呦提取的抗瘧新藥青蒿素的結構簡式,用鍵線式表示如圖.
2015年諾貝爾獎獲得者屠呦呦提取的抗瘧新藥青蒿素的結構簡式,用鍵線式表示如圖. ,需要在有機合成中引入羥基,引入羥基的反應類型有①②⑤.(選填編號)
,需要在有機合成中引入羥基,引入羥基的反應類型有①②⑤.(選填編號)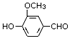 )可用于合成青蒿素,合成天然香草醛的反應如下:
)可用于合成青蒿素,合成天然香草醛的反應如下:
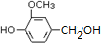 .
.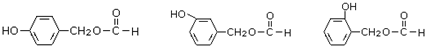 (其中之一).
(其中之一). 是合成青蒿素的中間原料之一,寫出由苯甲醛和氯乙烷為原料,制備芐基乙醛的合成路線流程圖(無機試劑任用).已知:羰基α-H可發生反應:
是合成青蒿素的中間原料之一,寫出由苯甲醛和氯乙烷為原料,制備芐基乙醛的合成路線流程圖(無機試劑任用).已知:羰基α-H可發生反應:
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

 或
或 .
.


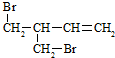
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
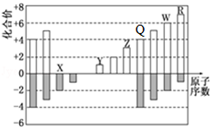
| A. | 原子半徑:Z>Y>X | |
| B. | X和Z形成的化合物能溶于NaOH溶液 | |
| C. | Q和X形成的化合物不能與酸反應 | |
| D. | R元素的含氧酸和W元素的含氧酸,酸性一定前者強 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com