
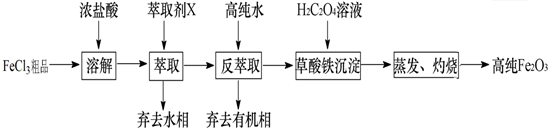
分析 (1)根據流程圖可知,FeCl3粗品溶于鹽酸,得到含有Fe3+、Ca2+、Mn2+、Cu2+等離子的溶液,用X萃取后再反萃取去掉有機相即可得到較純的含Fe3+的溶液,所以在萃取時Ca2+、Mn2+、Cu2+應在水相中,萃取劑X總量一定時,萃取的次數越多,效果越好,據此判斷;
(2)根據元素守恒可知,萃取后水相中鐵的存在形式是氯化鐵,用甲基異丁基甲酮萃取時,在有機相中鐵元素以形式存在HFeCl4,由于加高純水時,酸度[或c(H+)]降低,HCl(濃)+FeCl3?HFeCl4平衡向轉化為FeCl3的方向移動,所以用高純水可以進行反萃取;
(3)用冰水洗滌可以減少草酸鐵晶體的溶解損耗;
(4)在酸性條件下Fe2+與K2Cr2O7溶液反應生成Cr3+和鐵離子,根據電荷守恒和元素守恒書寫離子方程式;
(5)氧缺位體(CuFe2O4-a)可以奪取水分子了中的氧原子,從而生成氫氣,根據元素守恒書寫化學方程式;
(6)將鐵酸銅樣品在N2的氣氛中充分煅燒,減少的質量即為失去的氧元素的質量,根據CuFe2O4=CuFe2O4-a+$\frac{1}{2}$aO2可計算出a的值;
解答 解:(1)根據流程圖可知,FeCl3粗品溶于鹽酸,得到含有Fe3+、Ca2+、Mn2+、Cu2+等離子的溶液,用X萃取后再反萃取去掉有機相即可得到較純的含Fe3+的溶液,所以在萃取時Ca2+、Mn2+、Cu2+應在水相中,萃取劑X總量一定時,萃取的次數越多,效果越好,故選c,
故答案為:水;c;
(2)根據元素守恒可知,萃取后水相中鐵的存在形式是FeCl3,用甲基異丁基甲酮萃取時,在有機相中鐵元素以形式存在HFeCl4,由于加高純水時,酸度[或c(H+)]降低,HCl(濃)+FeCl3?HFeCl4平衡向轉化為FeCl3的方向移動,所以用高純水可以進行反萃取,
故答案為:FeCl3;加高純水時,酸度[或c(H+)]降低,HCl(濃)+FeCl3?HFeCl4平衡向轉化為FeCl3的方向移動;
(3)用冰水洗滌可以減少草酸鐵晶體的溶解損耗,
故答案為:減少草酸鐵晶體的溶解損耗;
(4)在酸性條件下Fe2+與K2Cr2O7溶液反應生成Cr3+和鐵離子,反應的離子方程式為6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O,
故答案為:6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O;
(5)氧缺位體(CuFe2O4-a)可以奪取水分子了中的氧原子,從而生成氫氣,反應的化學方程式為CuFe2O4-a+aH2O=CuFe2O4+aH2↑,
故答案為:CuFe2O4-a+aH2O=CuFe2O4+aH2↑;
(6)將鐵酸銅樣品在N2的氣氛中充分煅燒,減少的質量即為失去的氧元素的質量,根據CuFe2O4=CuFe2O4-a+$\frac{1}{2}$aO2可知$\frac{16a}{240}$×100%=1-96.6%,所以a=0.51,
故答案為:0.51.
點評 本題考查了物質分離提純的方法分析,涉及實驗基本操作、離子方程式的書寫、化學計算等知識,注意反應過程中原子守恒的理解應用,掌握基礎是關鍵,題目難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | 都具有強氧化性 | |
| B. | 分別露置在空氣中,容器內溶質的物質的量濃度都降低 | |
| C. | 常溫下都可以儲存于鋁制槽罐中 | |
| D. | 和碳反應中都表現出強氧化性和強酸性 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | K+、Ca2+、Cl-、CO32- | B. | Fe2+、Al3+、NO3-、SO42- | ||
| C. | Mg2+、NH4+、CO32-、H+ | D. | Na+、Br-、ClO-、H+ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
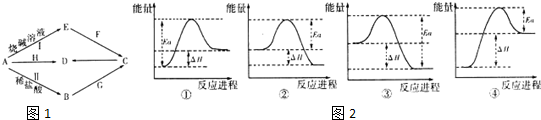
 ,實驗室制取G的化學方程式為Ca(OH)2+2NH4Cl=CaCl2+2NH3↑+2H2O.
,實驗室制取G的化學方程式為Ca(OH)2+2NH4Cl=CaCl2+2NH3↑+2H2O.| 化學鍵 | O=O(g) | H-H(g) | H-O(g) |
| 鍵能/kJ•mol-1 | 496 | x | 463 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
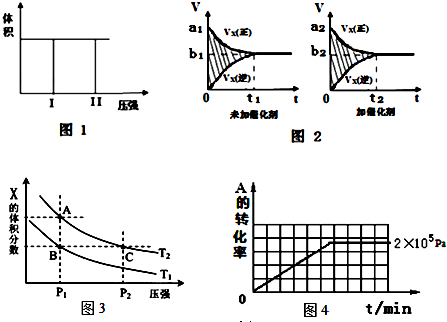
| 壓強p/Pa | 2×105 | 5×105 | 1×106 |
| c(A)/mol•L-1 | 0.08 | 0.20 | 0.44 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
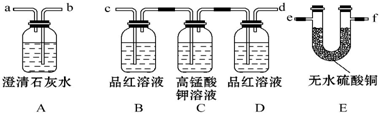
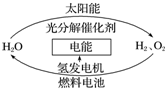 為消除目前燃料燃燒時產生的環境污染,同時緩解能源危機,有關專家提出了利用太陽能制取氫能的構想如圖所示.下列說法正確的是( )
為消除目前燃料燃燒時產生的環境污染,同時緩解能源危機,有關專家提出了利用太陽能制取氫能的構想如圖所示.下列說法正確的是( )| A. | 氫能源已被普遍使用 | |
| B. | H2O的分解反應是吸熱反應 | |
| C. | 氫氣不易貯存和運輸,無開發利用價值 | |
| D. | 2 mol 液態H2O具有的總能量高于2 mol H2和1 mol O2的能量 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 凡含有食品添加劑的食物對人體健康均有害,不宜食用 | |
| B. | 廢棄的塑料,金屬、紙制品及玻璃都是可回收再利用的資源 | |
| C. | 大氣污染物SO2、CO和NO2主要來源于煤的燃燒和汽車排放的尾氣 | |
| D. | 變質的油脂有難聞的特殊氣味,是由于油脂發生了化學變化 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com