
| A. | 在500℃、20 MPa條件下,在5 L密閉容器中進行合成氨的反應,使用催化劑后K增大 | |
| B. | 相同溫度下的酸、堿、鹽的稀溶液中水的離子積常數KW不同 | |
| C. | Ksp不僅與難溶電解質的性質和溫度有關,還與溶液中相關離子的濃度有關 | |
| D. | 室溫下K(HCN)<K(CH3COOH),等濃度的HCN和CH3COOH溶液pH較小的為CH3COOH |
分析 A、K是溫度的函數;
B、相同溫度下,水的離子積常數KW相同;
C、Ksp與難溶電解質的性質和溫度有關;
D、室溫下K(HCN)<K(CH3COOH),說明CH3COOH的電離度大于HCN的電離度.
解答 解:A、K是溫度的函數,使用催化劑平衡常數K不變,故A錯誤;
B、相同溫度下,水的離子積常數KW相同,而不是不同,故B錯誤;
C、Ksp與難溶電解質的性質和溫度有關,與溶液中的離子濃度無關,故C錯誤;
D、室溫下K(HCN)<K(CH3COOH),說明CH3COOH的電離度大于HCN的電離度,所以等濃度的HCN和CH3COOH溶液pH較小的為CH3COOH,故D正確;
故選D.
點評 本題綜合性較大,涉及平衡常數和水的離子積常數、溶度積常數等,比較基礎,旨在考查基礎知識的全面掌握情況,題目難度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:選擇題
| A. | 1:3 | B. | 1:1 | C. | 9:1 | D. | 3:1 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
| 實驗編號 | 反應物 | 催化劑 |
| ① | 10mL2% H2O2溶液 | 無 |
| ② | 10mL5% H2O2溶液 | 無 |
| ③ | 10mL5% H2O2溶液 | 1mL0.1mol•L-1FeCl3溶液 |
| ④ | 10mL5% H2O2溶液+少量HCl溶液 | 1mL0.1mol•L-1FeCl3溶液 |
| ⑤ | 10mL5% H2O2溶液+少量NaOH溶液 | 1mL0.1mol•L-1FeCl3溶液 |

查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
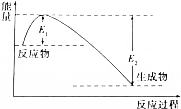 如圖所示的是1molNO2和足量的CO完全反應生成CO2和NO過程中的能量變化示意圖,能夠表示出CO2+NO=NO2+CO的能量變化示意圖的是( )
如圖所示的是1molNO2和足量的CO完全反應生成CO2和NO過程中的能量變化示意圖,能夠表示出CO2+NO=NO2+CO的能量變化示意圖的是( )| A. | 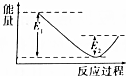 | B. | 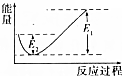 | C. | 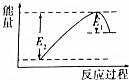 | D. | 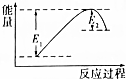 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
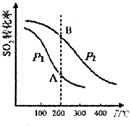 研究硫酸工業原理及含硫化合物的性質具有重要意義.
研究硫酸工業原理及含硫化合物的性質具有重要意義.| 氣體 | SO2 | O2 | SO3 |
| 濃度(mol•L-1) | 0.4 | 1.2 | 1.6 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com