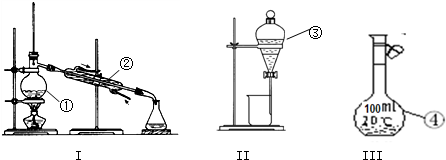
考點:溶液的配制,物質的分離、提純和除雜,物質的檢驗和鑒別的基本方法選擇及應用
專題:物質檢驗鑒別題,計算題
分析:(1)根據配置一定物質的量濃度的溶液所需操作步驟和每一步操作所需儀器分析;
(2)除去KCl溶液中的SO42-,應使SO42-離子轉化為沉淀,注意不能引入新的雜質;
(3)檢驗濾液中是否存在SO42-離子.
解答:
解:(1)配制一定物質的量的濃度的溶液需要稱量、溶解、洗滌、移液、定容等操作,溶解需要燒杯、玻璃棒,定容需要膠頭滴管、需要100mL容量瓶進行配制,故答案為:燒杯,玻璃棒,100 mL容量瓶 膠頭滴管;
(2)除去KCl溶液中的SO42-,應先加入過量BaCl2使SO42-生成沉淀,然后加入K2CO3使過量的BaCl2生成沉淀,過濾后加入HCl除去過量的K2CO3,
故答案為:BaCl2、K2CO3、HCl;
(3)檢驗濾液中是否存在SO42-離子,用氯化鋇通過生成硫酸鋇來檢驗,具體操作為:取所得溶液的上層清液1~2滴于滴定板上,再滴入1-2滴BaCl2溶液,若溶液未變渾濁,則表明SO42-已沉淀完全.
故答案為:取所得溶液的上層清液1~2滴于滴定板上,再滴入1-2滴BaCl2溶液,若溶液未變渾濁,則表明SO42-已沉淀完全.
點評:本題考查物質的分離、提純的基本方法選擇與應用,題目難度中等,注意根據混合物組分性質的差異性選擇分離的方法,本題易錯點為(2),注意加入試劑的順序和除雜原理.